Ergänzende Informationen zu Adler et al.; auch diese Zusammenfassung ist noch nicht allgemein verständlich aufbereitet:
Warinner C et al. (2104): Pathogens and host immunity in the ancient human oral cavity. Nature Genetics 46, 336,344, doi:10.1038/ng.2906
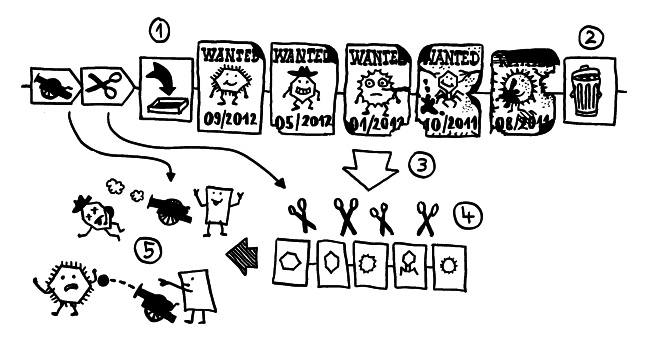
Zahnstein enthält viele verwertbare Informationen (DNA, Proteine) und ist in vielen alten Schädeln zu finden. Die Autoren haben (1) die Mundflora von mittelalterlichen Menschen mit leichter bis schwerer Parodontitis analysiert, (2) 40 opportunistische Pathogene charakterisiert, (3) alte mutmaßliche Atibiotikaresistenzgene identifiziert, (4) das Genom des Parodontitis-assoziierten Keims Tannerella forsythia rekonstruiert und (5) 239 bakterielle sowie 43 menschliche Proteine identifiziert, die einen historisch alten Zusammenhang zwischen Faktoren unseres Immunsystems, Pathogenen des „roten Komplexes“ und Parodontitis belegen.
Die humane Mundflora umfasst über 2000 Bakterien-Taxa, darunter viele Keime, die an Parodontitis, Atemwegs-, kardiovaskulären und systemischen Erkrankungen beteiligt sind. Zahnstein = komplexer, mineralisierter Biofilm, der aus Zahnbelag (Plaque), Speichel und der Flüssigkeit in Zahnfleischtaschen entsteht.
Adler et al. haben die alte Mundflora nur auf Phylumebene analysiert und gezielt nach einigen Arten gesucht. Zur Charakterisierung des Gesundheitszustands wurden hier nun an vier Skeletten aus dem mittelalterlichen Kloster Dalheim (Deutschland, etwa 950-1200 n. Chr.) genauere Analysen durchgeführt. 2699 mikrobielle OTUs (operational taxonomic units) identifiziert. Dominant: 1 Archäen- und 9 Bakterien-Phyla (mit absteigenden Anteilen: Firmicutes, Actinobacteria, Proteobacteria, Bacteroidetes, Synergistetes, Chloroflexi, Fusobacteria, Spirochetes, Euryarchaeota), die alle auch moderne Mundflora dominieren. Bemerkenswert selten: Bodenbakterien wie Acidobacteria -> kaum Verunreinigung der Proben. Weiterlesen