Am Ende des letzten Beitrags habe ich das Protein HLA-G erwähnt, mit dem der Trophoblast – die Kontaktfläche des Embryos zum mütterlichen Gewebe – die Immunzellen in der Gebärmutter friedlich stimmt und für die nötigen Umbaumaßnahmen im Adernetz rekrutiert.
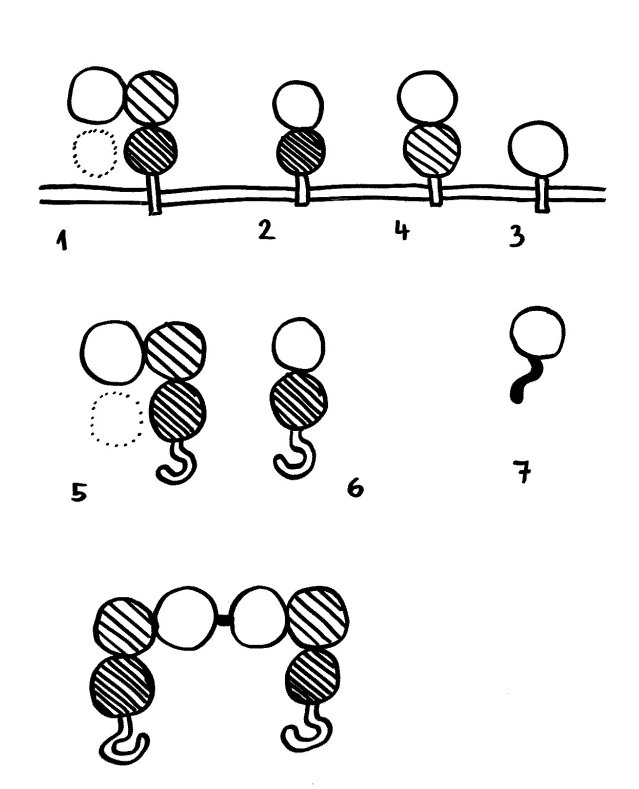
Die klassischen HLA-Moleküle wie HLA-A sind extrem polymorph, d. h. es gibt zahlreiche leicht unterschiedliche Varianten, da diese Moleküle die Aufgabe haben, Abermillionen unterschiedlicher Antigen-Bruchstücke zu binden und den Immunzellen zu präsentieren. HLA-G weist einen viel geringeren Polymorphismus auf und hat entsprechend andere Funktionen. Sein Gen liegt – wie das von HLA-A – im Haupthistokompatibilitätskomplex (MHC) auf Chromosom 6. Man kennt vier membrangebundene Formen (G1 bis G4) und drei lösliche (G5 bis G7).
Die membrangebundenen Formen können aber durch Enzyme von der Zelloberfläche abgeschnitten werden und den Zellen dann ebenfalls als lösliche Signalstoffe dienen. Einige der Formen können sich zu Dimeren zusammenlagern (s. Abb.: unten ein Dimer aus zwei HLA-G5-Molekülen).