Vor einem Jahr erschien eine Arbeit über das Mikrobiom unkontaktierter Yanomami, die ich damals nur kurz besprechen konnte. Jetzt habe ich sie noch einmal gelesen, obwohl sie immunologisch unergiebig ist: Die Entnahme von Blutproben, die Aufschluss über den Zustand des Immunsystems dieser Menschen hätte geben können, war bei einem Erstkontakt selbstverständlich unmöglich. Man muss schon froh sein, dass sie Abstriche aus ihrer Mundschleimhaut und das Einsammeln von Stuhlproben gestattet haben – vermutlich nicht, ohne sich über dieses merkwürdige Verhalten zu amüsieren.
Die Hauptergebnisse: Die Bakteriengemeinschaften auf der Haut und im Stuhl dieser mutmaßlich seit über 11.000 Jahren isolierten Menschen sind erheblich artenreicher als unsere – und auch als die Mikrobiome anderer naturnah lebender Völker. Die sogenannte Alpha-Diversität ihrer Mikrobiome ist also sehr hoch, vermutlich, weil sie nie mit antimikrobiellen Substanzen zu tun hatten und weil sie in ständigem Kontakt mit ihrer Umwelt leben. In ihrer Darm- und Hautflora leben zum Beispiel Bakterien, die man bislang für reine Bodenbakterien gehalten hat. Zugleich sind die Unterschiede in der Mikrobiom-Zusammensetzung zwischen den 34 Yanomami, von denen die Proben stammen, viel geringer als zwischen denen zweier Menschen aus einer Gruppe aus unserem Kulturkreis. Die sogenannte Beta-Diversität ist mithin sehr klein – wohl wegen des engen Zusammenlebens, der hygienischen Verhältnisse und der gleichartigen Lebensweise und Ernährung aller Gruppenmitglieder.
Unter den Genen dieser Bakterien, und zwar überweigend den Genen von zuvor unbekannten Stämmen des Darmbakteriums Escherichia coli, finden sich 28, die Antibiotika-Resistenzen vermitteln – sogar gegen einige neue, synthetische Antibiotika. Allerdings werden diese Gene in den Bakterien nicht abgelesen, sie sind „stummgeschaltet“ (silenced), sodass die Bakterien anfangs dennoch auf die Antibiotika ansprechen würden. Aber man muss damit rechnen, dass sie sehr bald wirklich Resistenzen entwickeln würden, und zwar gleich gegen mehrere Antibiotika. In Weltgegenden und Kulturen, in denen die sogenannte Therapietreue (die regelmäßige Einnahme des Medikaments über den kompletten notwendigen Zeitraum) vermutlich gering ist, geht das umso schneller.
Erstkontakt: Es gibt keinen Weg zurück
Dem Forscherteam war bewusst, dass die Probensammlung beim Erstkontakt eine einmalige Gelegenheit ist, ein Mikrobiom-Archiv anzulegen, das vermutlich große strukturelle und funktionale Ähnlichkeiten mit dem Mikrobiom unserer altsteinzeitlichen Vorfahren hat – auch wenn sich die einzelnen Bakterien-Arten und -Stämme natürlich auf dem Weg ihrer Wirte nach und durch Südamerika weiterentwickelt haben. 11.000 Jahre entsprechen ungefähr 100 Millionen Bakteriengenerationen. Zugleich begann mit dieser Begegnung zwischen der bislang isolierten Dorfgemeinschaft und den Medizinern und Wissenschaftlern unwiderruflich der Niedergang dieser Diversität – spätestens mit der ersten Antibiotika-Gabe.
Die Autoren schreiben in ihrer Danksagung: „Wir sind auch den Leuten in dem neu kontaktierten Dorf dankbar für ihr Vertrauen und für unser gemeinsamen Wunsch, dass der unvermeidliche Kontakt mit unserer Kultur ihrem Volk gesundheitliche Vorteile und Schutz bringen möge.“ Ist das nicht ein arg frommer Wunsch angesichts der bisherigen Erfahrungen mit der gesundheitlichen und sozialen Entwicklung neu kontaktierter, kleiner indigener Gruppen?
Von 230 indigenen Gruppen in Brasilien wurden 87 in dem guten halben Jahrhundert zwischen 1900 und 1957 ausgelöscht. Die indigene Gesamtpopulation Brasiliens ist seit 1500 auf schätzungsweise ein Zwanzigstel geschrumpft. Die Lebenserwartung indigener Brasilianer und Venezuelaner liegt unter der von Sierra Leone im Jahr 2000. Sind gezielte Kontaktaufnahmen angesichts dieser Katastrophen überhaupt ethisch vertretbar, und was gilt es dabei und danach zu beachten?
Zugang zur modernen Medizin: Fluch oder Segen?
Die Meinungen zum Gesundheitszustand isolierter indigener Gruppen gehen weit auseinander, und die Positionen scheinen sich oftmals aus Werthaltungen zu speisen, die von den Fakten nicht unbedingt gedeckt sind. Exemplarisch seien hier zwei Arbeiten vorgestellt.
A. M. Hurtado et al. geben in ihrer 2005 erschienenen Arbeit „Human Rights, Biomedical Science, and Infectious Diseases Among South American Indigenous Groups“ einen Überblick. Die wenigen Daten, die wir überhaupt haben, wurden naturgemäß alle erst nach dem Erstkontakt erhoben, und sie sind nicht leicht zu interpretieren. So konstatieren die Autoren eine sehr starke Th2-Dominanz des Immunsystems vieler Indigener und oftmals enorm hohe IgE-Werte, also Konzentrationen jener Antikörper, die bei uns mit Allergien und Asthma assoziiert sind. Daraus leiten sie ab, dass man unbedingt ihre Th1-Abwehr stärken müsse, damit sie Viren- und Bakterien-Infektionen besser verkraften – und zwar, indem man sie von ihren Parasiten befreit, also entwurmt.
Dabei sind IgE-Werte nur sogenannte Surrogat-, also Ersatzparameter für den schwieriger zu ermittelnden Parasitenbefall, und der Parasitenbefall ist seinerseits ein Surrogatparameter für das, was uns eigentlich interessiert: den Gesundheitszustand der Menschen. Wie sich in den letzten Jahren gezeigt hat, kann man auch mit Würmern im Darmtrakt symptomfrei und fit sein; ja, ein moderater Befall mit Würmern, die seit Jahrtausenden eine Koevolution mit den Menschen durchlaufen, scheint vor einigen gefährlicheren Parasiten und vor schädlichen Überreaktionen des Immunsystems zu schützen.
Ungefähr drei Viertel der Yanomami, die man untersucht hat, sind mit Würmern der Gattung Necator befallen. Trichuris fand sich bei 96 Prozent einer Yanomami-Gruppe, Ascaris bei ausnahmslos allen Angehörigen einer anderen. Sehr viele Yanomami sind mit Hepatitis-Viren infiziert; auch andere Viren wie Influenza machen ihnen zu schaffen. All diese Epidemien sind allerdings – anders als die Würmer – erst nach dem Erstkontakt aufgetreten und gerade deshalb ein Problem. Dem Vorschlag der Autoren zur Verbesserung der Gesundheit durch rigorose Parasitenbekämpfung zu folgen hieße, sehr tief in das Leben der Menschen einzugreifen – sie etwa in feste Siedlungen mit sanitären Anlagen umzusiedeln, um den Kreislauf der Reinfektion mit Würmern über die oral-fäkale Route zu durchbrechen. Ob dies wirklich ihren Interessen entspricht und ethisch geboten ist, wie die Autoren meinen, darf m. E. angesichts der historischen Erfahrungen kritisch diskutiert werden.
Am anderen Ende des Spektrums stehen P. Carrera-Bastos et al. mit ihrer 2011 erschienenen Arbeit „The western diet and lifestyle and diseases of civilization“, auf die sich Anhänger der sogenannten Paleo-Diät berufen. Sie betonen, dass sogenannte Zivilisationskrankheiten wie koronare Herzkrankheiten, Adipositas, Bluthochdruck, Typ-2-Diabetes oder Autoimmunerkrankungen in Jäger-und-Sammler-Gesellschaften selten bis inexistent seien, weil ihre Ernährung, ihre Lebensweise und ihre Physiologie evolutionär aneinander und an unsere natürliche Umwelt angepasst sind.
Der auch im Alter noch niedrige Blutdruck, die anhaltend hervorragende Insulinsempfindlichkeit, der niedrige BMI, das dünne Unterhautfettgewebe, das große Lungenvolumen, die Seltenheit von Fehlsichtigkeit, die geringe Osteoporoseneigung usw. sind in der Tat beeindruckend. Andererseits verringern die hohe Kindersterblichkeit und Todesfälle durch Konflikte, Unfälle usw. die mittlere Lebenserwartung. Dennoch soll ein Alter von 68 bis 78 Jahren nichts Ungewöhnliches gewesen sein. Gesundheitsförderlich waren bzw. sind neben vielseitiger, frischer Kost viel Tageslicht, viel Bewegung, ein an den Tag-Nacht-Rhythmus angepasstes Schlafverhalten, akuter statt chronischer Stress sowie das Fehlen schädlicher synthetischer Substanzen.
Aber auch hier gilt: Wir wissen es im Grunde nicht, sondern können nur versuchen, den „Urzustand“ anhand der Beobachtungen nach dem Erstkontakt und auf Basis von Fossilien zu rekonstruieren. Vermutlich gibt es gar nicht den Urzustand, sondern eine erhebliche Varianz in der Gesundheit und den Lebenserwartungen. Auch Blutdruck, Blutzucker- oder Leptinwerte usw. sind zunächst einmal Messerwerte, die sich nicht ohne Weiteres in Morbidität und Mortalität ummünzen lassen. Und dann müssen wir immer noch abwägen: zum einen verschiedene gesundheitliche Aspekte, etwa Kindersterblichkeit gegen Zivilisationskrankheiten. Und zum anderen die möglichen Vorteile einer engmaschigen medizinischen Betreuung gegen die damit einhergehenden soziale Umbrüche und ihre Folgen.
Was heißt schon „unkontaktiert“?
Im Grunde gibt es kaum noch wirklich unkontaktierte indigene Gruppen. Im Amazonas-Becken zum Beispiel können sich Infektionen über den Handel zwischen indigenen Gruppen ausbreiten. Durch die Abholzung, die Anlage neuer Plantagen, das Drogengeschäft und den Goldbergbau gelangen zahlreiche Arbeiter in die Wälder. Das Wasser wird mit Schwermetallen belastet, die selbst schwere Krankheiten auslösen oder den Organismus so schwächen können, dass bis dahin leicht zu überwindende Infektionen schlechter verkraftet werden. Und die örtlichen Mückenpopulationen können beim Blutsaugen an infizierten Arbeitern Pathogene wie Malaria-Erreger aufnehmen und dann auf Indigene übertragen.
Ist das Kind erst einmal in den Brunnen gefallen, ist schnelle medizinische Hilfe und ein langfristiges Monitoring der Gruppen vonnöten.
Aber wieso sind Indigene überhaupt so anfällig für viele Infektionen? Warum sind seit der Eroberung Amerikas so viel mehr amerikanische Ureinwohner ansteckenden Krankheiten zum Opfer gefallen als Europäer?
Virgin Soil Epidemics
Auf ihrer langen Reise aus Afrika über Eurasien nach Nord- und schließlich Südamerika haben die Urahnen der heute dort lebenden indigenen Gruppen zahlreiche evolutionäre Flaschenhälse durchlaufen: Die ohnehin kleinen Gründerpopulationen wurden mit neuen Selektionsdrücken konfrontiert und schrumpften stark, bevor sie sich stabilisieren konnten. Ein solches Evolutionsmuster, der sogenannte serial founder effect, führt zu einer Reduzierung der genetischen Vielfalt – auch im Genpool des Immunsystems. Die an sich extrem polymorphen, also vielgestaltigen Gene im Haupthistokompatibilitätskomplex zum Beispiel sind in Südamerika viel variantenärmer als in Europa oder gar in Afrika. Und das heißt: Einem neuartigen Erreger, der ein Mitglied einer Population erkranken lässt, haben vermutlich auch die anderen Mitglieder keine hinreichende Widerstandskraft entgegenzusetzen.
Außerdem halten Afrikaner, Europäer und Asiaten seit Jahrtausenden Nutzvieh, mit dem sie wegen des engen Kontakts zahlreiche Pathogene, aber auch gutartige Mikroorganismen ausgetauscht haben. Ihr Immunsystem ist an diesem ständigen Zustrom von Bakterien, Viren, Pilzen, Einzellern und Würmern geschult worden – sowohl stammes- als auch individualgeschichtlich.
Zudem leben viele Indigene Südamerikas in kleinen, isolierten Gruppen. In Nordamerika, Europa und Asien ist die Bevölkerungsdichte viel höher. Daher konnten sich in Südamerika fast nur solche Pathogene halten, die ihre Wirte nicht umbringen, sondern mit ihnen koexistieren – denn sie können nicht beliebig oft auf den nächsten Wirt überspringen, sobald der alte „verbraucht“ ist. In Weltgegenden mit größerer und dichterer Bevölkerung hat sich dagegen zusätzlich zu diesen alten Parasiten und Pathogenen ein neuer Typus von Krankheitserregern herausgebildet, der seine Wirte entweder umbringen kann oder immun werden lässt. Er breitet sich wellenförmig in großen Populationen aus, verursacht also Epidemien. Die Nachfahren von Überlebenden solcher Epidemien haben bei den nächsten Runden einen ererbten Überlebensvorteil. Wo solche „modernen“ Viren und Bakterien bislang unbekannt waren, etwa wegen zu kleiner und isolierter Populationen, begegnet das Immunsystem ihnen dagegen hilflos. Die Menschen dort sind für die Erreger virgin soil, also jungfräulicher Boden: Neuland.
Turbo-Tuberkulose bei den Aché
Zwar litten auch die Europäer nach Kolumbus‘ Fahrten unter Krankheiten, die aus der Neuen Welt eingeschleppt worden waren; man denke nur an die Syphilis. Aber aus den genannten drei Gründen starben – relativ gesehen – in der Folge des Pathogen-Austauschs sehr viel mehr indigene Amerikaner als Europäer. Und aus denselben Gründen sind isolierte indigene Gruppen noch heute nach dem Erstkontakt äußerst gefährdet.
Besonders eindringlich ist das Beispiel der Northern Aché in Paraguay, die nur wenige Jahre nach ihrer „Entdeckung“ und gewaltsamen Umsiedlung in den 1970er-Jahren von einer Tuberkulose-Epidemie heimgesucht wurden. Nur sechs Jahre nach dem Erstkontakt hatten 18 Prozent von ihnen aktive Tuberkulose, und zwei Drittel aller Erwachsenen waren mit dem Erreger Mycobacterium infiziert.
Bei europäischen Infizierten dauert es meist Jahre, bis die Krankheit zum Ausbruch kommt, und dann noch einmal viele Jahre, bis man an ihr stirbt. Ihren Höhepunkt erreichten die Tuberkulose-Epidemien in Europa im frühen 19. Jahrhundert und in Nordamerika im frühen 20. Jahrhundert. Nicht nur verbesserte hygienische Verhältnisse, sondern auch die erbliche Widerstandskraft der Epidemie-Überlebenden gegen die Infektion trugen zum Rückgang der Krankheit bei.
In Südamerika konnte Mycobacterium wegen der kleinen Bevölkerungsgruppen lange nicht Fuß fassen. Kommen Indigene mit Menschen in Kontakt, die – teils ohne es zu wissen – eine chronische, mild verlaufende Tuberkulose haben, so stecken sie sich sehr leicht an. Die Krankheit bricht auch sehr bald aus und verläuft bei ihnen völlig anders, als wir es aus Europa kennen: Unbehandelt sterben viele von ihnen, und der Hauttest, mit dem normalerweise auf Tuberkulose getestet wird, versagt bei den meisten, da ihr Immunsystem kaum auf die Erreger reagiert.
Die ersten Aché mit aktiver Tuberkulose wurden 1992 mit dem Arzneimittel Isoprodian behandelt, das von einem deutschen Pharmaunternehmen hergestellt wird. Es war vor seinem Einsatz in keiner einzigen klinischen Studie untersucht worden. Das Therapieregime sah eine Einnahme über zwölf Monate hinweg vor, und zwar entweder in Kliniken, die viele Meilen von den Siedlungen der Aché entfernt lagen, oder aber in ihren Siedlungen, die wiederum für das medizinische Personal schwer erreichbar waren. Die Wege waren oft überflutet, und die Patienten konnten sich die regelmäßige Anreise nicht leisten. Zudem verstanden sie das Konzept hinter dieser Behandlung kaum. Entsprechend schlecht war ihre Therapietreue: Viele nahmen das Mittel unregelmäßig und nicht lang genug ein. Bei einem Drittel versagte die Therapie. In einer solchen Situation breiten sich rasch resistente Keime aus, gegen die das Medikament auch dann nicht mehr ankommt, wenn es ordnungsgemäß eingenommen wird. Wenn man die Durchführung einer Therapie nicht an die örtlichen Lebensumstände anpasst und die Gemeinschaften nicht langfristig und engmaschig betreut, bereitet man der nächsten Epidemie den Weg.
Epidemien im Amazonasgebiet: Es wird besser
Die gute Nachricht, wenn man so will: Erst wird es schlimm, dann wird es besser. Die Mortalitätsraten fallen mit der Zeit – weil die Überlebenden der Virgin-Soil-Phase ihre Widerstandsfähigkeit vererben und weil die Verständigung und die medizinische Versorgung nach und nach besser werden. Eine Übersichtsarbeit aus dem Jahr 2015 stellt Daten aus 117 Epidemien in 59 indigenen Gruppen im Amazonasgebiet zusammen, denen zwischen 1875 und 2008 über 11.000 Menschen zum Opfer gefallen sind. Drei Viertel der Todesfälle gehen auf Masern, Grippe und Malaria zurück. Die höchsten Mortalitätsraten dieser Epidemien lagen bei 83, 97 und 74 Prozent. Solche Verheerungen rauben kleinen, traditionell lebenden Gruppen jede soziale Struktur und jedes wirtschaftliche Fundament.
Über alle Epidemien gemittelt, lag die Mortalitätsrate 1963 noch bei 24 Prozent pro Jahr und 2015 bei 10 Prozent pro Jahr. Es kann jedoch auch dramatische Rückschläge geben, etwa wenn die lokale Bevölkerungsdichte durch Umsiedlungen in Reservate steigt oder wenn die medizinische Versorgung wegbricht. So haben Missionare den Stamm der Yora sechs Monate lang betreut; dann brachen sie zu einem Heimaturlaub auf. Einige Wochen später waren Dutzende ihrer „Schützlinge“ tot. Ähnlich lief es 1975 bei den Aché.
Nicht immer ist die medizinische Versorgung entscheidend: Gegen manche Infektionskrankheiten bildet sich rasch eine natürliche Immunität aus, sobald erst einmal fast alle Mitglieder der Gruppe infiziert sind und sich immer wieder gegenseitig anstecken. Die Dörfer der brasilianischen Yanomami werden erst seit der Ankunft von Gold-Prospektoren im Jahr 1987 von Malaria heimgesucht. Dennoch haben die Menschen dort, wo die Malaria stabil ist, also ganzjährig häufig übertragen wird, rasch gute Immunreaktionen gegen den Erreger entwickelt. Wo die Malaria dagegen instabil ist, also nur gelegentlich eine Epidemie aufflackert, sind die Symptome stärker, und die Sterblichkeit ist höher.
Allergien und Autoimmunerkrankungen nahezu unbekannt
Wie eingangs erwähnt, dürfte neben den Lebensumständen und genetischen Prädispositionen der indigenen Gruppen auch die Th2-Dominanz in ihrem Immunsystem die Anfälligkeit für Epidemien fördern: Ihr System ist an den Befall mit Würmern und Einzellern angepasst und hält diese Parasiten mit einer dauerhaft hohen Produktion von Antikörpern des Typs IgE, als einer starken humoralen Abwehr in Schach. Der andere Arm der erworbenen Immunität, der Th1-Weg oder die zelluläre Abwehr, ist bei ihnen entsprechend schwach ausgeprägt, denn diese beiden Abwehrmechanismen hemmen sich gegenseitig.
Entsprechend selten sind Allergien, Asthma und Autoimmunerkrankungen bei indigenen Gruppen. Multiple Sklerose beispielsweise tritt bei den Lakadoniern, einer Ethnie in Mexiko, überhaupt nicht auf: Unter 5372 untersuchten Personen gab es keinen einzigen Fall.
Eine Ausnahme von dieser Regel ist der endemische Pemphigus foliaceus, eine Autoimmunerkrankung der Haut, die in Brasilien als fogo selvagem bezeichnet wird und lokal gehäuft und stets in Verbindung mit einem Gewässer auftritt. Der Auslöser der Angriffe des Immunsystems auf einen Bestandteil der Haut ist – wie bei so vielen Autoimmunerkrankungen – unbekannt. Einer Hypothese zufolge lösen die Bisse eines Insekts die Attacken aus; eine andere mögliche Ursache ist Methylquecksilber, das im Amazonasbecken in großem Stil zur Goldgewinnung eingesetzt wird und den Boden und die Flüsse verseucht.
Versucht man nun den Th1-Arm des Immunsystems zu stärken, indem man die Menschen entwurmt und das Risiko eines erneuten Befalls senkt, werden Allergien und Autoimmunerkrankungen bei ihnen vermutlich häufiger auftreten. Diese Risiken zu erhöhen und zugleich das Risiko tödlicher Infektionen (etwa mit HIV) zu verringern, kann natürlich dennoch ein guter Deal sein. Aber ganz ohne unbeabsichtigte Nebenwirkungen wird ein solcher Eingriff in das evolutionäre Gleichgewicht zwischen Parasiten und ihren Wirten nicht bleiben – ganz abgesehen von Fragen nach der langfristigen Wirksamkeit von Entwurmungen und nach den sozialen Folgen der tiefgreifenden Veränderung der Wohn- und Lebensverhältnisse, die zur Unterbrechung der Infektionszyklen notwendig sind. Platt gesagt: Eine entwurmte Indigene, die sich in einer Elendssiedlung prostituiert, hat kein geringeres, sondern ein höheres Risiko, an Aids zu erkranken.
Lasst sie in Ruhe
All das ist kein Problem der Vergangenheit: Man erwartet, dass in nächster Zukunft über 50 isolierte Gruppen im Amazonasbecken mit der Außenwelt in Kontakt kommen werden. Wie es im Rest der Welt aussieht, zeigt der englische Wikipedia-Artikel über nicht kontaktierte Gruppen – von „Völkern“ will ich bei Restpopulationen von oftmals wenigen Dutzend Menschen lieber nicht sprechen.
Nach zahlreichen verheerenden Epidemien und anderen Ereignissen, die zum Tod oder zur Verelendung von Indigenen geführt haben, ist man inzwischen weltweit zu der Einsicht gelangt, dass man sie am besten in Ruhe lässt, solange sie nicht von sich aus den Kontakt suchen – oder unfreiwillig von rücksichtslosen Personen kontaktiert und vermutlich auch kontaminiert wurden.
Allerdings bleibt das ein frommer Wunsch, solange die zuständigen nationalen Behörden ineffizient oder korrumpierbar sind und andererseits übermächtige finanzielle Interessen ins Spiel kommen – und das ist im Amazonasbecken fast überall der Fall. Etwas einfacher ist der Schutz von Menschen, die wirklich isoliert leben, etwa auf Inseln. North Sentinel Island, eine Insel der Andamanen im Indischen Ozean, hat zum Beispiel keine Bodenschätze, und die Bewohner haben bei fast jedem dokumentierten Kontaktversuch mit Pfeil und Bogen unmissverständlich klar gemacht, dass sie in Ruhe gelassen werden wollen. (Die einzige bekannte Ausnahme: eine auf Film gebannte Bootstour mit Kokosnüssen als Gastgeschenk. Auch das wäre heute nicht mehr zulässig.)
Wir wissen nicht, warum die Sentinelesen Kontaktversuche ablehnen und ob sie irgendetwas vom Schicksal der anderen Negritos auf den Andamanen mitbekommen haben. Wir wissen auch nicht das Geringste über ihre Ernährung, ihre Lebenserwartung, ihr Mikrobiom und ihr Immunsystem. Bei aller Wissbegierde und aller Hoffnung auf eine Verbesserung unserer Gesundheit durch die Erforschung indigener Gruppen, die kaum Autoimmunerkrankungen kennen – angesichts dieser Zahlen ist zu hoffen, dass sie noch lange isoliert bleiben:
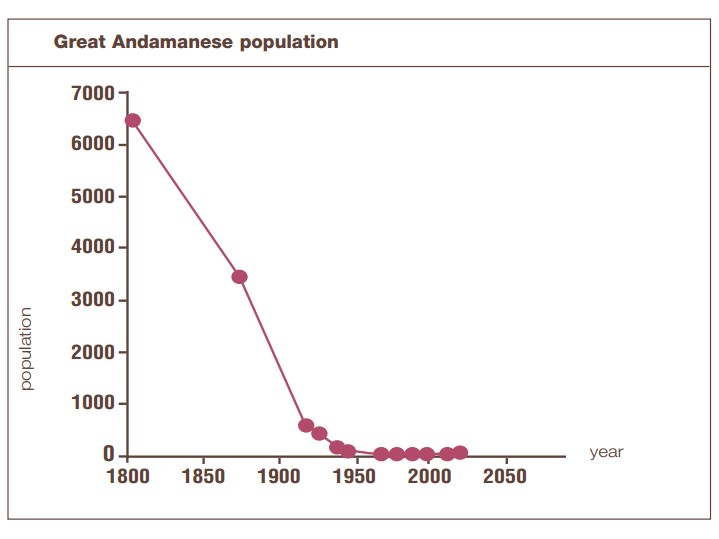
Aus: Progress can kill, © Survival International 2007. Quelle: Venkatesan, D. 1990. Ecocide or Genocide? The Onge in the Andaman Islands. Cultural Survival Quarterly 14(4), 49-51.
Literatur
Carrera-Bastos P et al.: The western diet and lifestyle and diseases of civilization. Research Reports in Clinical Cardiology 2011:2 15-35 (PDF).
Clemente JC et al.: The microbiome of uncontacted Amerindians. Science Advances 2015:1(3) e1500183.
Flores J et al.: Absence of Multiple Sclerosis and Demyelinating Diseases among Lacandonians, a Pure Amerindian Ethnic Group in Mexico. Multiple Sclerosis International 2012, 292631.
Gillings MR et al.: Ecology and Evolution of the Human Microbiota: Fire, Farming and Antibiotics. Genes 2015:6(3) 841-857.
Hurtado AM et al.: Longitudinal Study of Tuberculosis Outcomes Among Immunologically Naive Aché Natives of Paraguay. American Journal of Physical Anthropology 2003:121 134-150 (PDF).
Hurtado, AM et al.: Human rights, biomedical science, and infectious diseases among South American indigenous groups. Annual Review of Anthropology, 2005:34 639-665.
Marcano TJ et al.: Cross-sectional Study Defines Difference in Malaria Morbidity in Two Yanomami Communities on Amazonian Boundary between Brazil and Venezuela. Mem Inst Oswaldo Cruz, Rio de Janeiro, 2004:99(4) 369-376 (PDF).
Robledo MA: Chronic methyl mercury poisoning may trigger endemic pemphigus foliaceus “fogo selvagem”. Medical Hypotheses 2012:78(1) 60-66.
Survival International: Progress can kill. How imposed development destroys the health of tribal people. Broschüre, 2007 (PDF).
Walker RS et al.: Mortality from contact-related epidemics among indigenous populations in Greater Amazonia. Scientific Reports 2015:5 14032.

Toller informativer Text über spannende Zusammenhänge. Aber ich meine irgendwo über einem PC-Bildschirm den Spruch gelesen zu haben: „Dies wird keine Doktorarbeit!“ 🙂