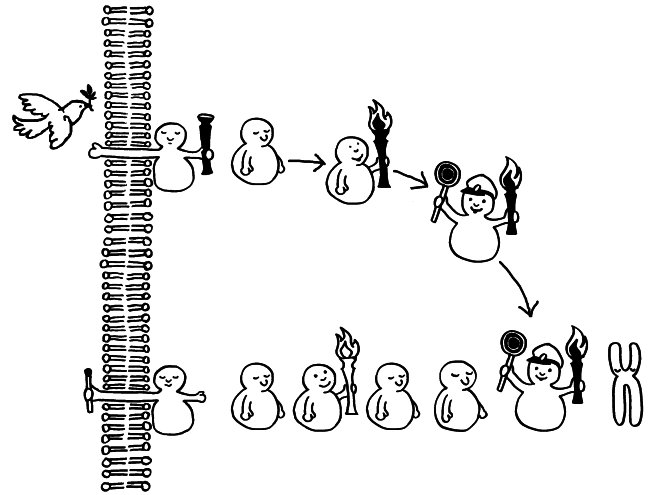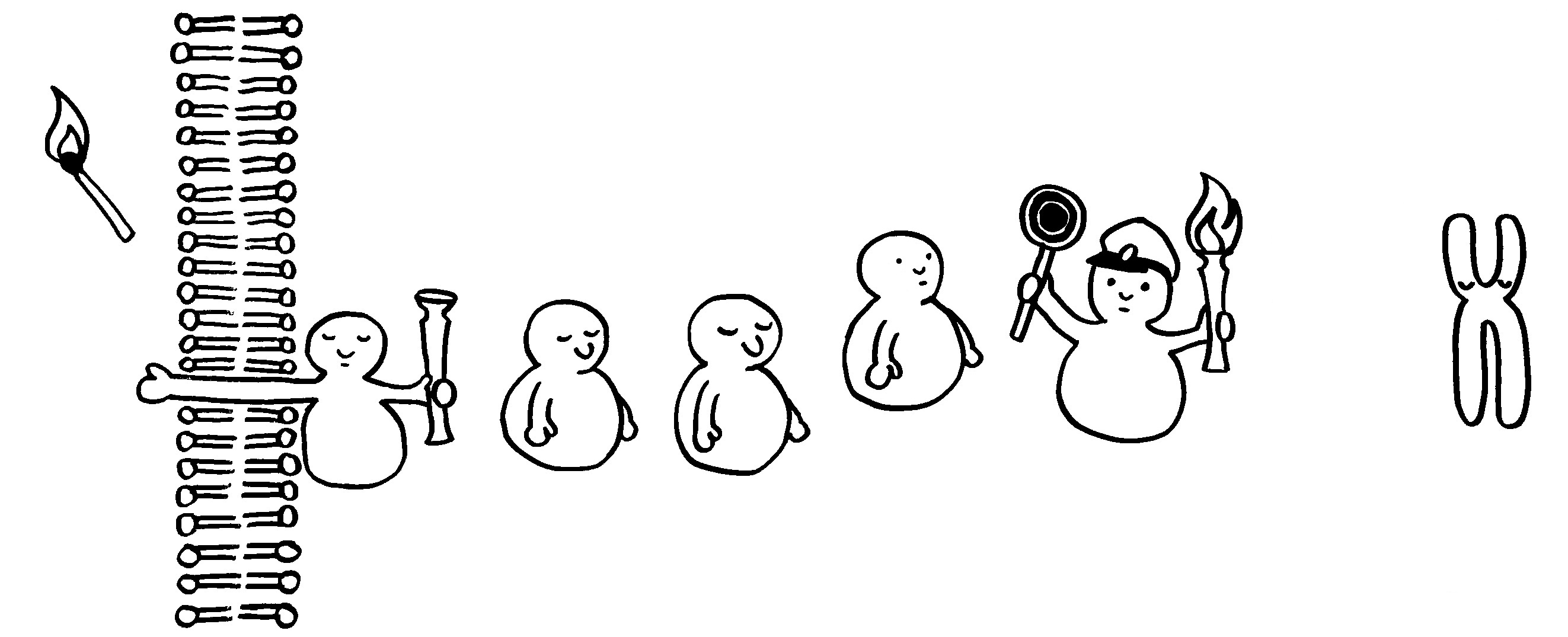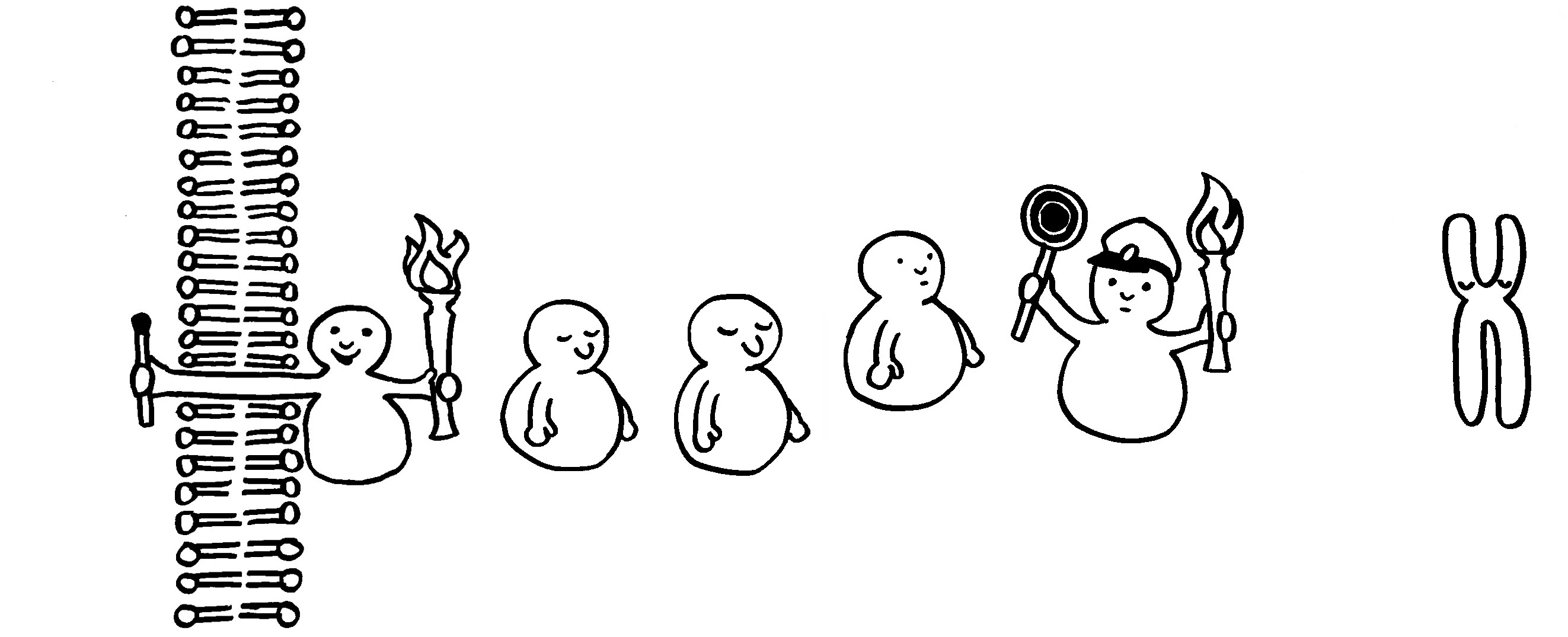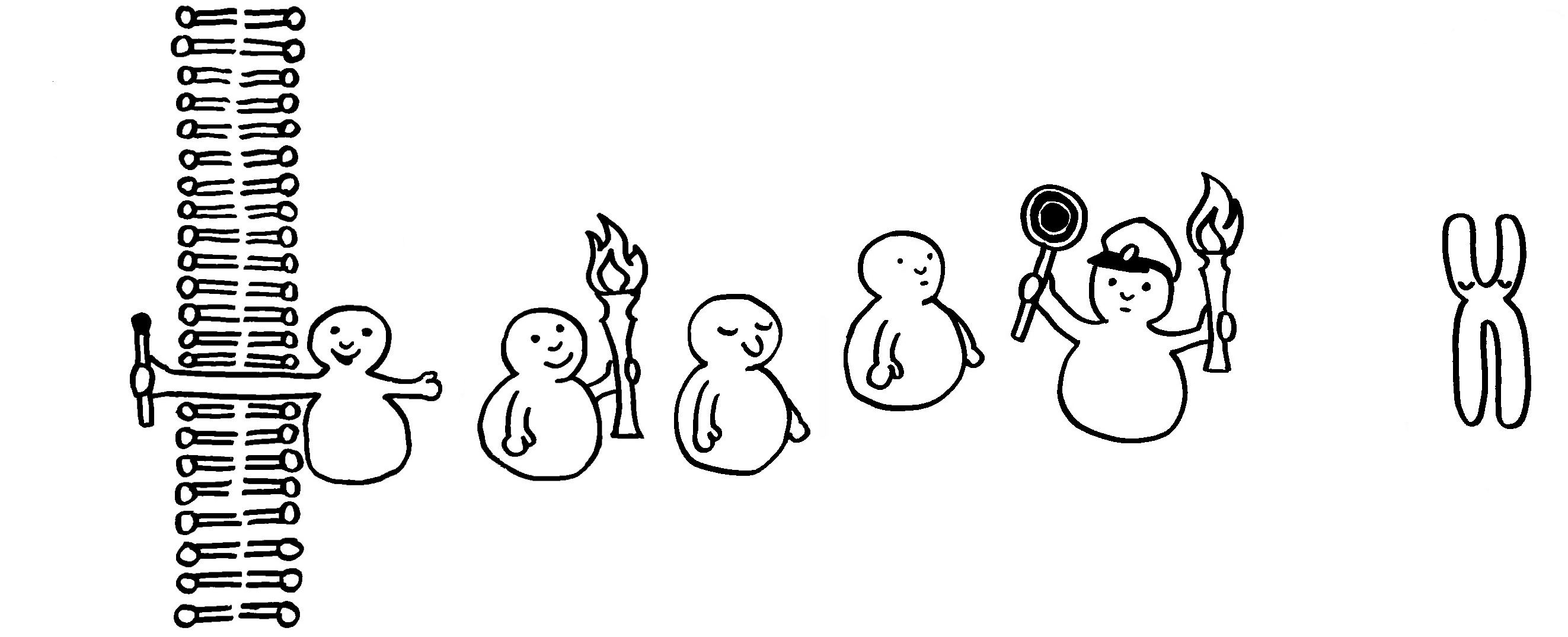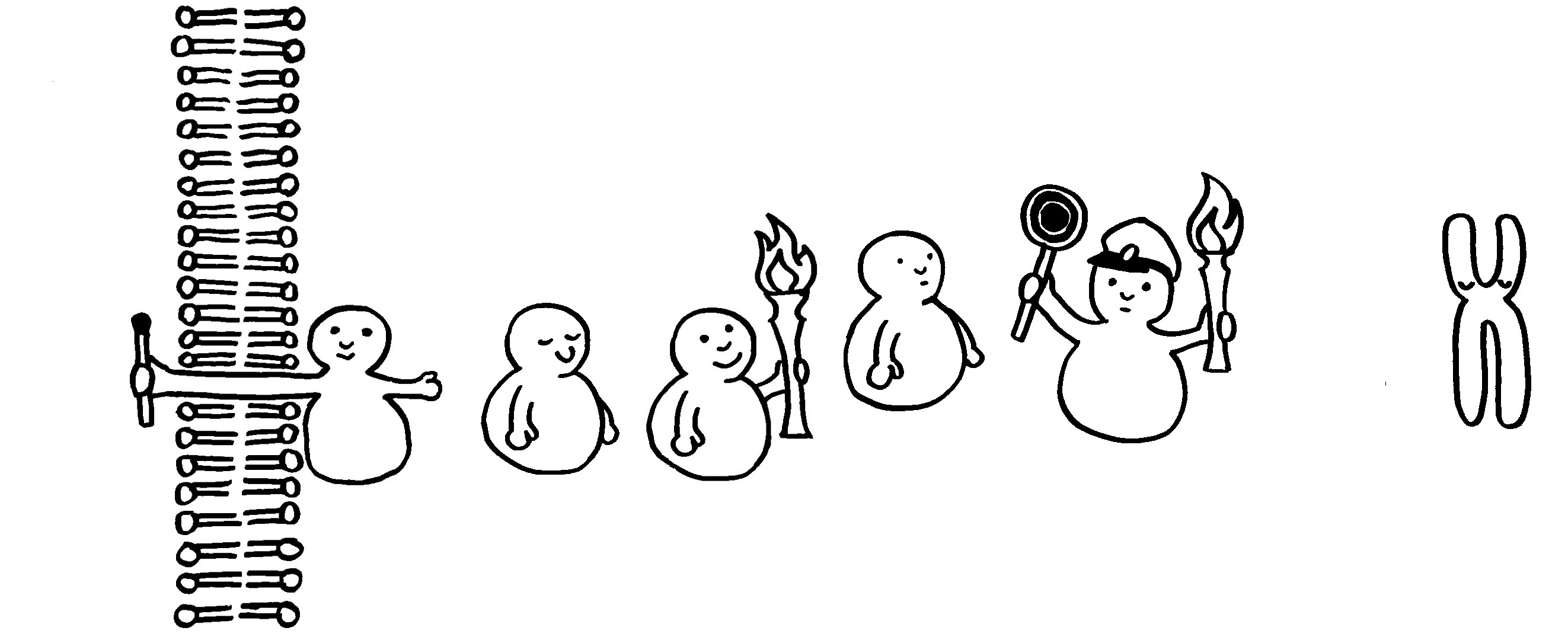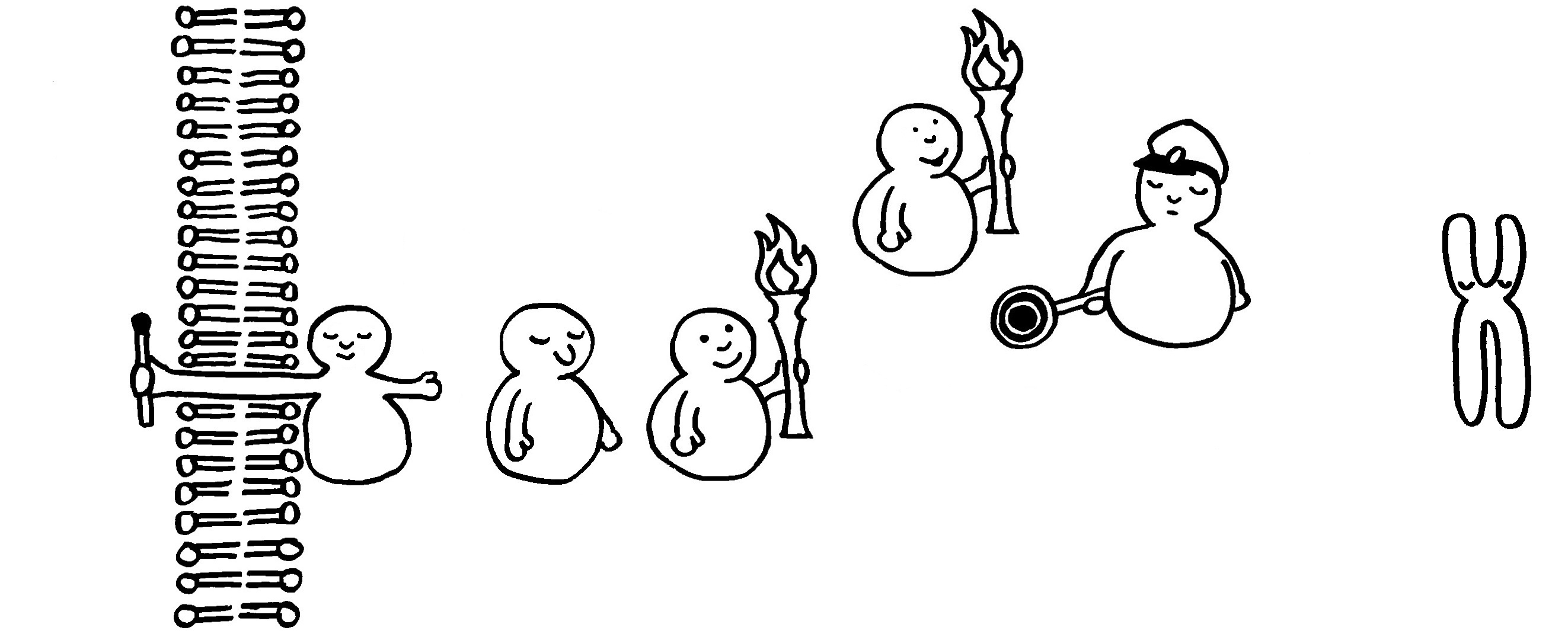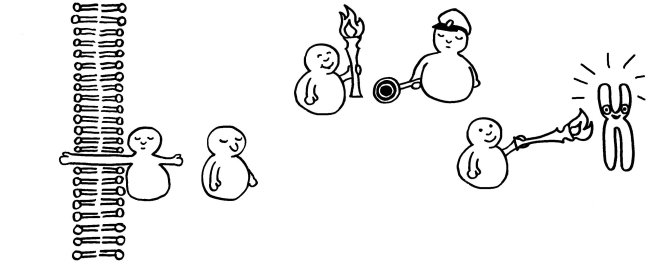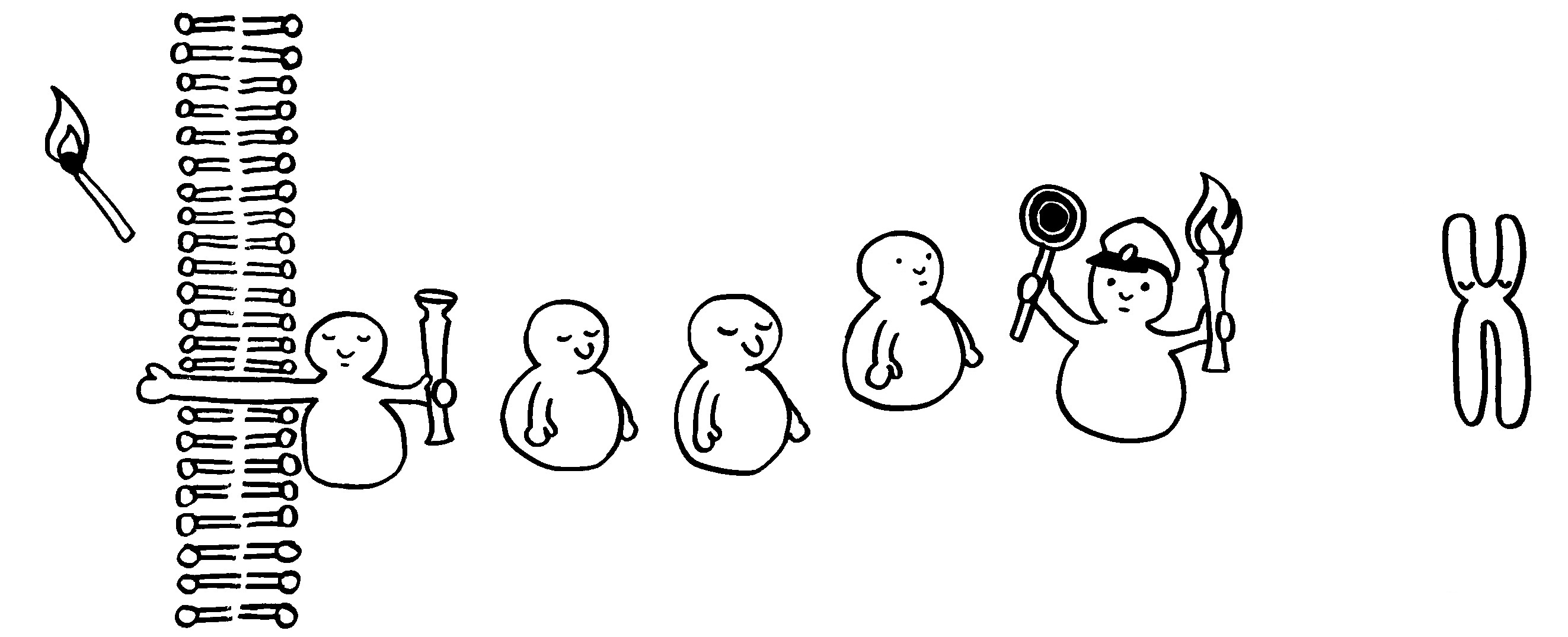
Solange ein Rezeptor in der Membran einer Immunzelle keinen Liganden gebunden hat, ruht die innerzelluläre Signalkette. Ein Inhibitor blockiert den Zugang zum Zellkern.
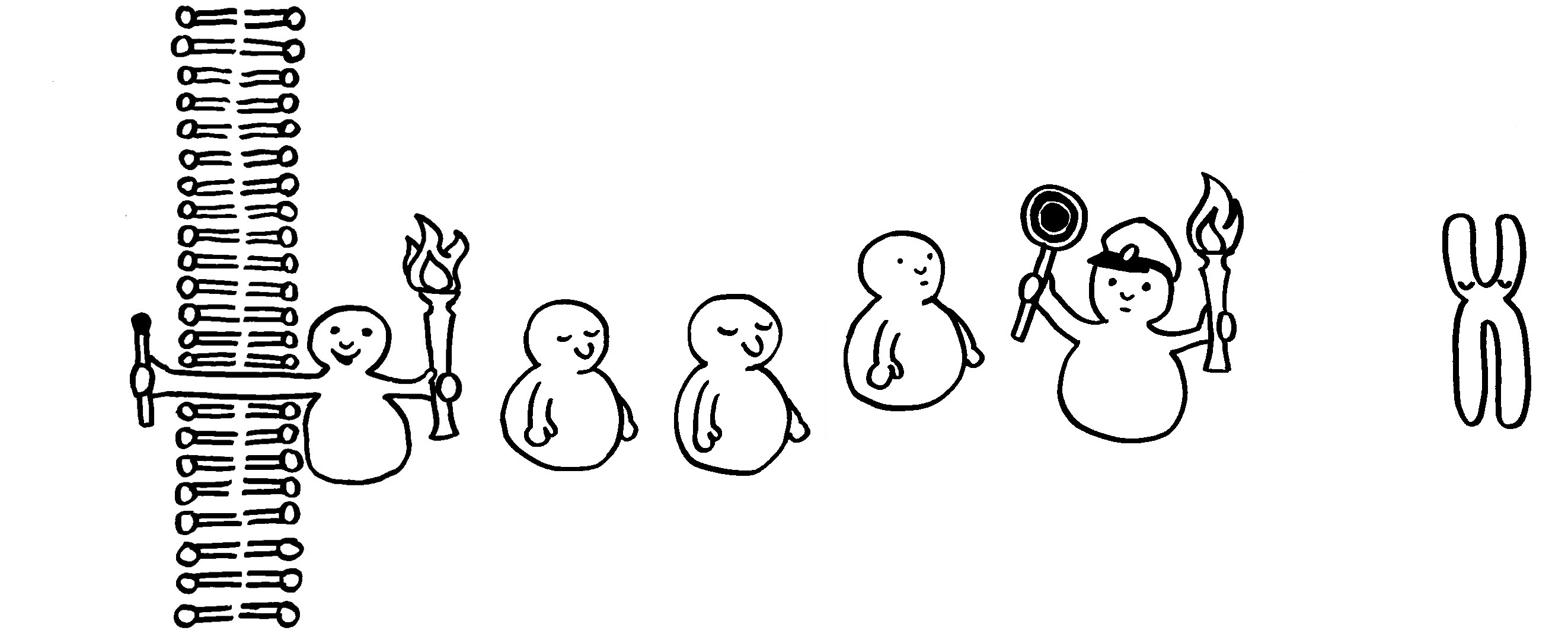
Die Bindung des Liganden – etwa eines Zytokins, das auf eine Infektion hinweist – aktiviert den Rezeptor. Dessen Innenseite ist dann bereit, das Signal an das nächste Glied in der Kette weiterzureichen.
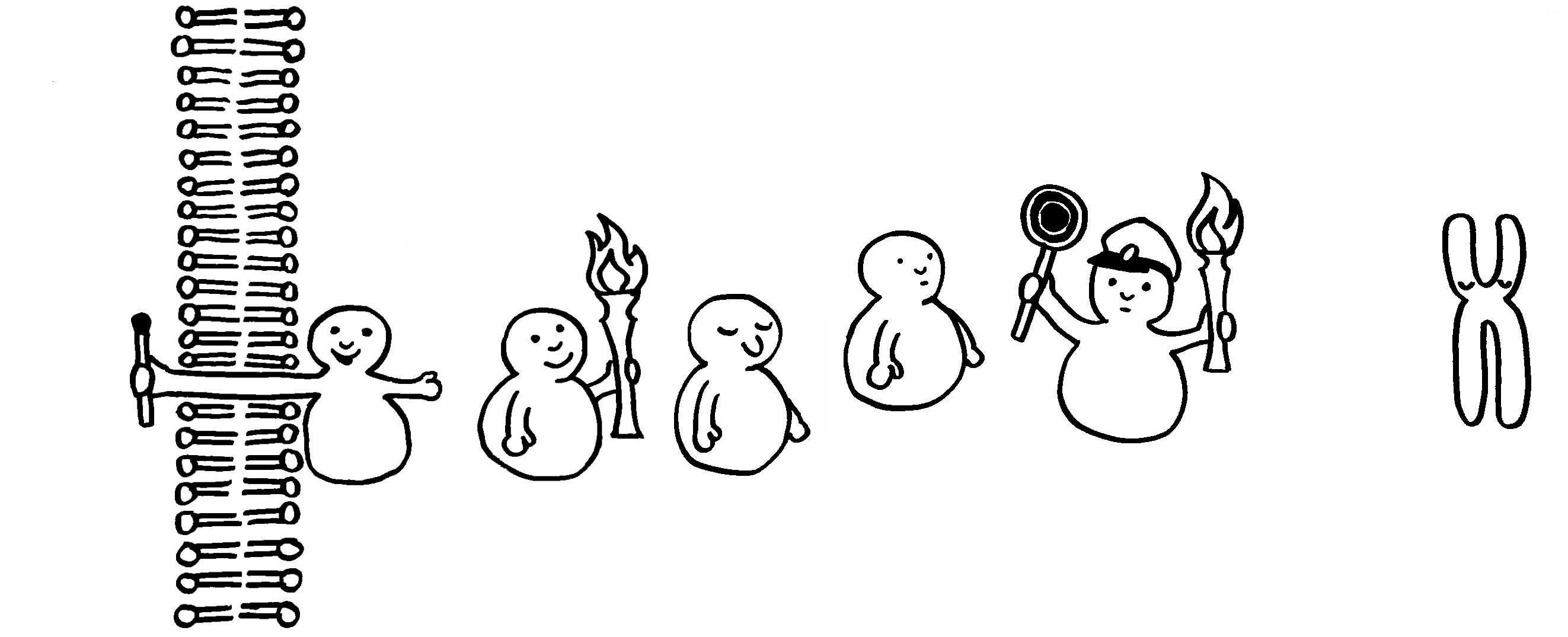
Eine Kinase wird durch Übernahme einer Phosphatgruppe (Fackel) aktiviert.
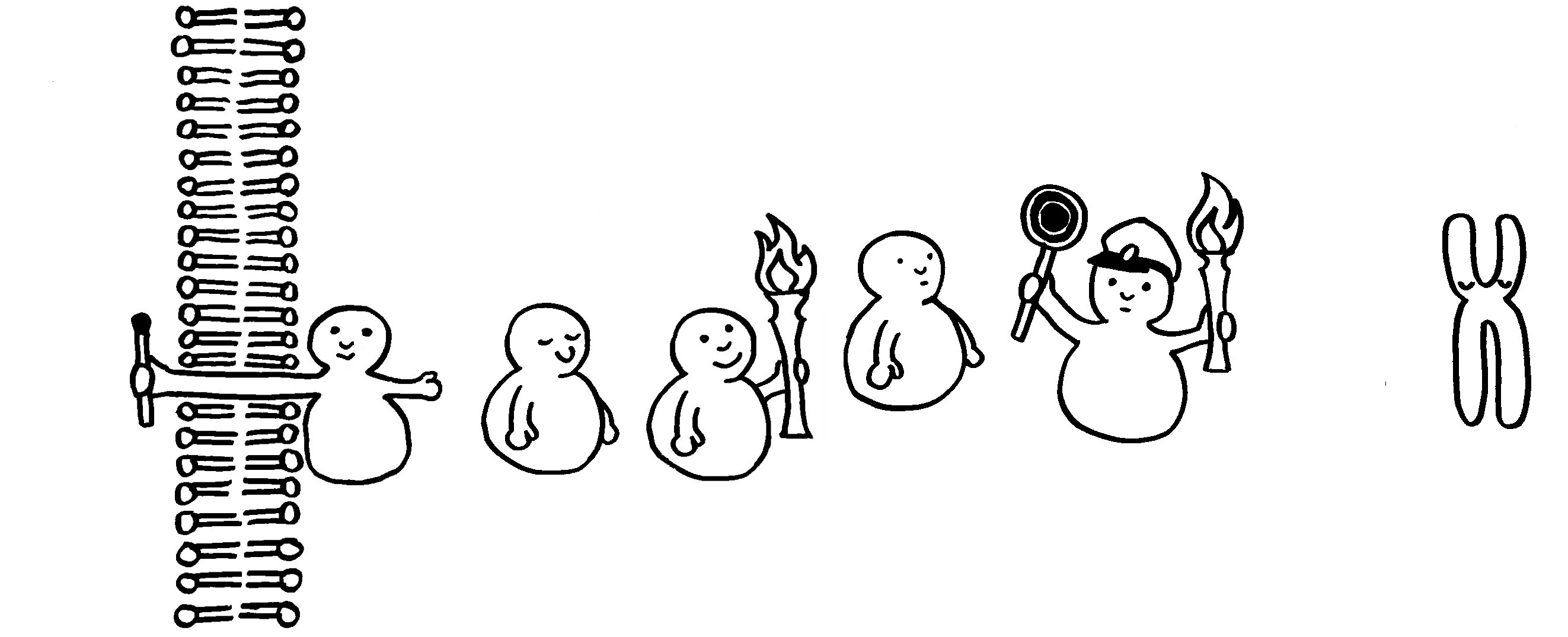
Sie aktiviert ihrerseits die nächste Kinase usw. (Weitergabe der Fackel).
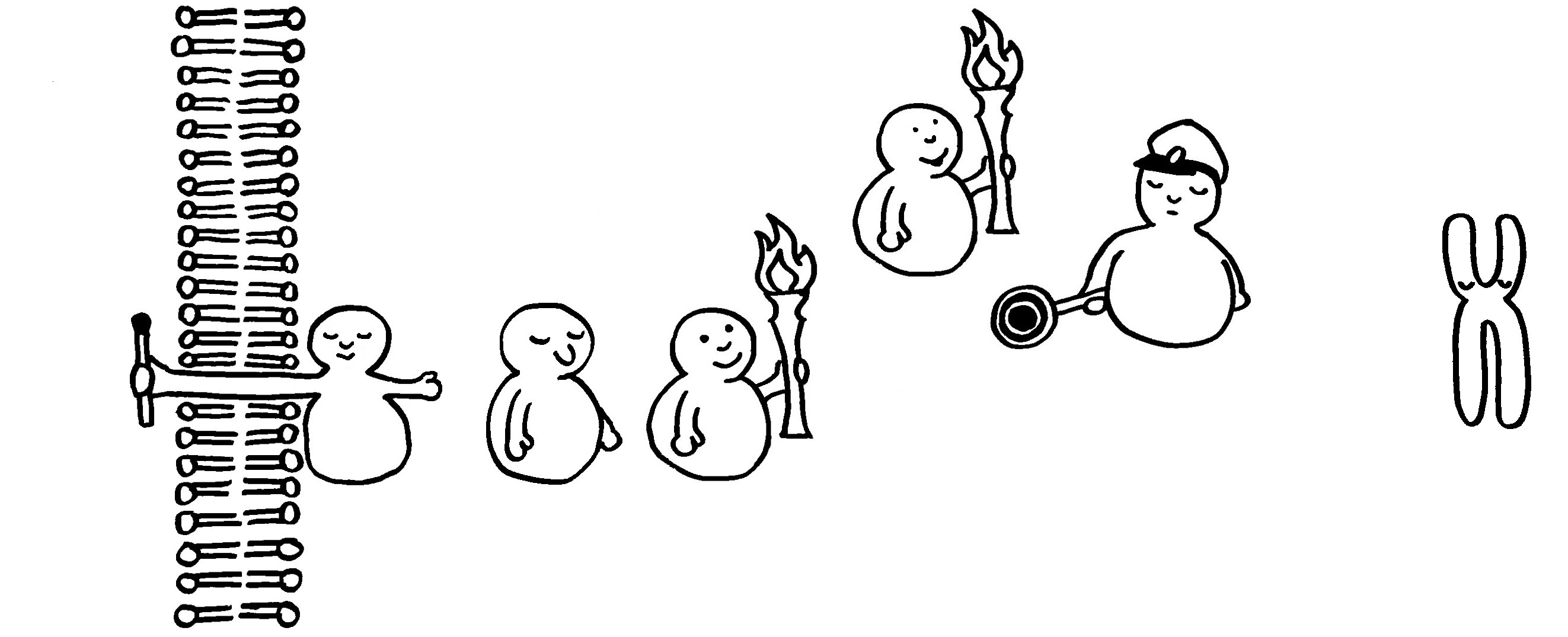
Auch Phosphatasen können sich an solchen Signalketten beteiligen, etwa indem sie einem Inhibitor eine Phosphatgruppe abnehmen und ihn dadurch ausschalten.
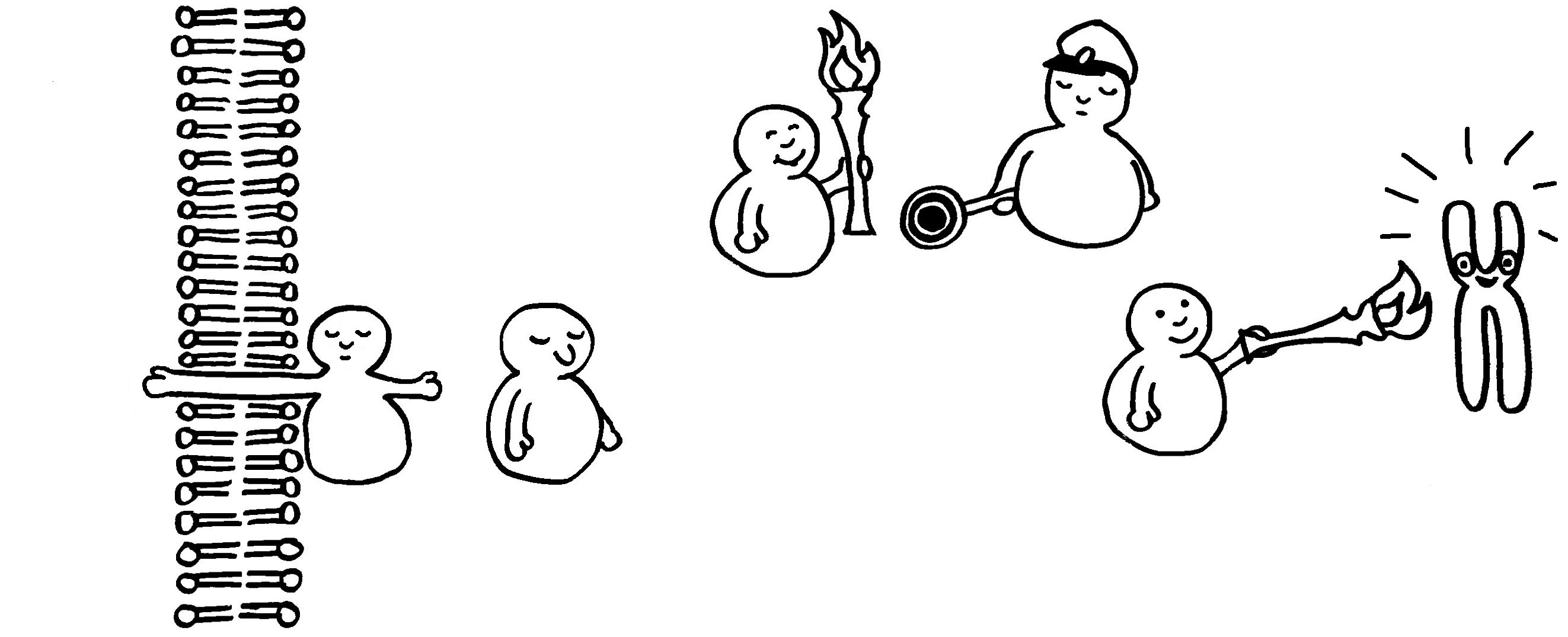
Am Ende erreicht das Signal ein Chromosom im Zellkern. Von diesem werden dann beispielsweise Gene abgelesen, deren Produkte an einer Abwehrreaktion beteiligt sind.
Sie dürfen diese Zeichnung gerne in Folien etc. übernehmen, sofern Sie die Quelle angeben: Dr. Andrea Kamphuis, https://autoimmunbuch.de