Schon lange ist bekannt, dass aktivierte Zellen des Immunsystems mithilfe von Lockstoffen an die Stelle gelotst werden, an der sie benötigt werden – etwa an den Ort einer Infektion, im Fall einer Influenza also zu den virenbefallenen Epithelzellen der Atemwege. Allerdings sind diese Stoffe, Chemokine genannt, löslich; sobald sie in die Gewebsflüssigkeit oder in die Blutbahn ausgeschüttet wurden, werden sie verdünnt oder fortgespült. Daher hat man sich lange gefragt, wie beispielsweise zytotoxische T-Zellen bei einer Grippe so schnell an genau die richtige Stelle gelangen.
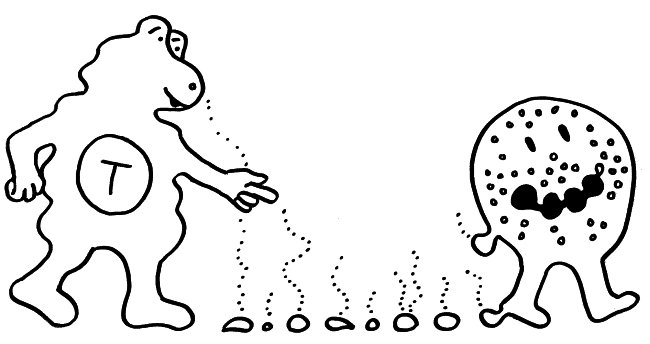
Ein Forscherteam um Kihong Lim hat jetzt herausgefunden, dass die Neutrophilen – jene Zellen der angeborenen Anwehr, die als „erste Verteidigungslinie“ gegen eine Influenza besonders früh am Infektionsort eintreffen – bei ihrem geschäftigen Kommen und Gehen eine Art Membran-Schleppe ausbilden, von der sie ständig kleine Membransäckchen abschnüren, die mit dem Chemokin CXCL12 gefüllt sind. Sie legen gewissermaßen Brotkrumenspuren, die umso dichter sind, je näher der Infektionsort ist – einfach aufgrund der Zahl der dort verkehrenden Neutrophilen, ähnlich wie die Duftstraßen der Ameisen in der Nähe des Nests oder einer Nahrungsquelle.
Das Chemokin diffundiert dann langsam aus den Membrankügelchen heraus und steigt den sich nähernden T-Zellen gewissermaßen als Duft in die Nase: Es bindet an deren CXCL12-Rezeptor.
In Mäuse ohne Neutrophile werden die zytotoxischen T-Zellen bei einer Influenza-Infektion zwar aktiviert, aber sie finden die mit den Viren infizierten Zellen in der Luftröhre nur ganz schlecht und bekämpfen die Infektion daher sehr ineffizient.
Literatur:
Kihong Lim et al.: Neutrophil trails guide influenza-specific CD8+ T cells in the airways. Science, 4. September 2015, Vol. 349, no. 6252, DOI: 10.1126/science.aaa4352