Im Lauf der nächsten Monate extrahiere ich aus Band 1 einige Vortragsthemen – das ist wegen der Zeichnungen sinnvoller als reine Lesungen. Den Anfang macht eine etwa 40 Minuten lange, allgemein verständliche und angstfreie Einführung in die Arbeit unserer unterschiedlichen Immunzellen – angstfrei, weil nicht Krankheiten, sondern die normalen Tätigkeiten der Zellen im Fokus stehen.
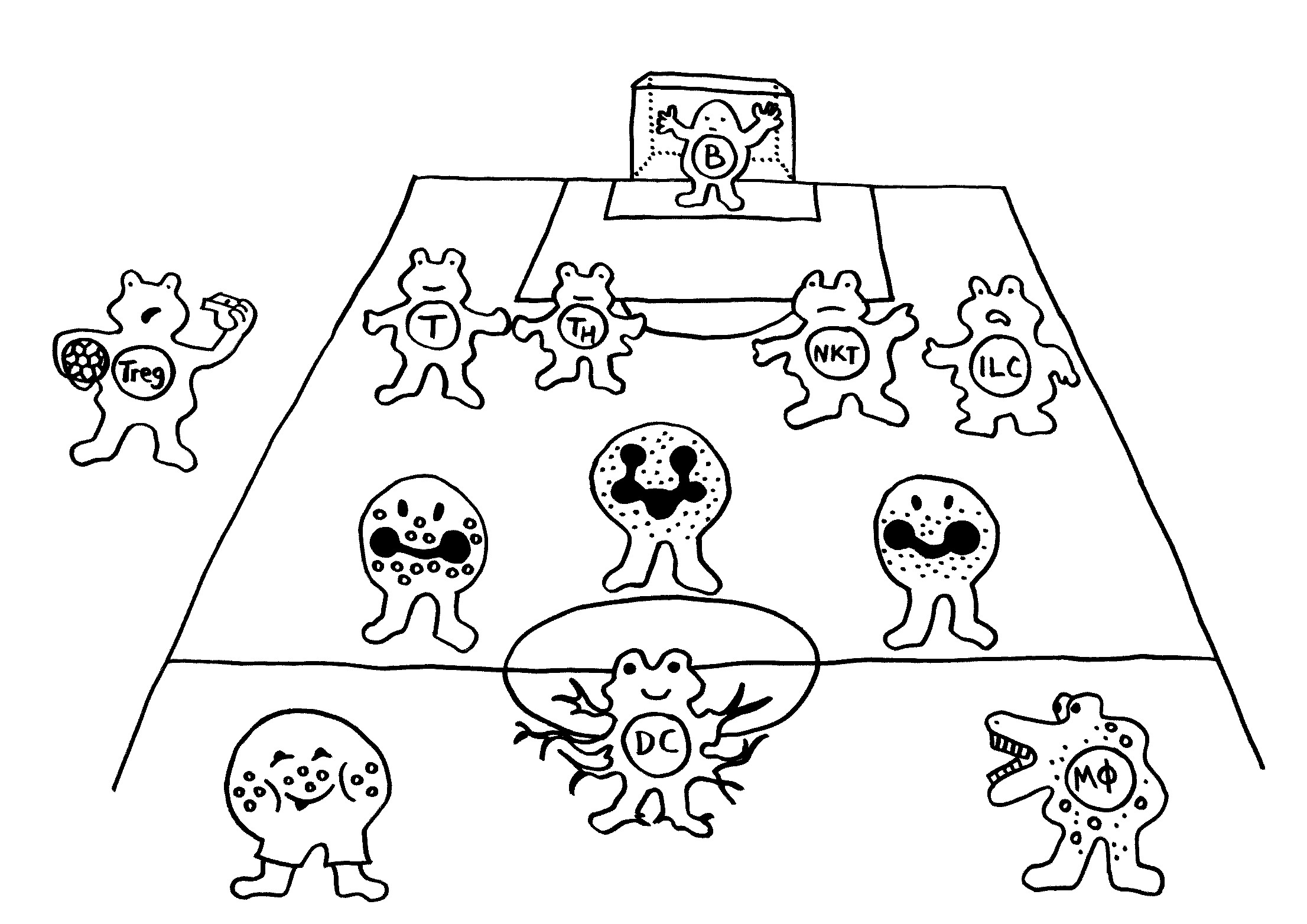
Der Vortrag hangelt sich an 15 Karikaturen entlang, die ich in kleinerer Runde als A2-Blätter an eine Tafel hängen und in größerer Runde auf eine Leinwand projizieren kann. Vortragsanfragen (etwa von Selbsthilfegruppen) schicken Sie bitte an kontakt@immunbuch.de.