Neulich las ich, dass selbst schwaches Nachtlicht eine Brustkrebstherapie u. U. wirkungslos machen kann, weil das Licht die nächtliche Melatoninproduktion stört, was wiederum die Tumorzellen stärkt. Beim Nachrecherchieren führte eins zum anderen, und zack: Schon muss das Autoimmunbuch um ein Kapitel erweitert werden. Wie die sogenannte circadiane Rhythmik – das Schwingen aller möglicher Abläufe in unserem Körper mit einer Periode von etwa 24 Stunden – und der nächtliche Schlaf unser Immunsystem regeln, ist nämlich hochspannend und auch für Autoimmunerkrankungen relevant.
Von dem Dutzend Arbeiten, die ich zum Thema gelesen habe, empfehle ich vor allem die Übersicht „T Cell and Antigen Presenting Cell Activity During Sleep“ von Tanja Lange und Jan Born (2011), auf der die meisten der folgenden Abbildungen basieren.
Wie stellt das Immunsystem sicher, dass sich entzündungsfördernde und entzündungshemmende Signale, die angeborene und die erworbene Abwehr sowie der Th1- und der Th2-Arm der erworbenen Abwehr nicht ins Gehege kommen? Durch räumliche und zeitliche Trennung: Der Tag gehört den entzündungshemmenden Signalen, der angeborenen Abwehr und denjenigen Zellen der erworbenen Abwehr, die Pathogene unmittelbar bekämpfen: den zytotoxischen T-Zellen. Und in der Nacht – vor allem, wenn man schläft und nicht durchwacht – dominieren Entzündungsreaktionen, die uns tags bei lebensnotwendigen Aktivitäten stören würden. Außerdem wird nachts durch die Kontakte zwischen antigenpräsentierenden Zellen und T-Helferzellen das immunologische Gedächtnis angelegt.
Hormone aus der Zirbeldrüse und der Hypophyse im Gehirn sowie aus der Nebennierenrinde, deren Ausschüttung von der zentralen inneren Uhr im Hypothalamus gesteuert wird, sorgen dafür, dass die richtigen Zellpopulationen zu jeder Zeit am richtigen Ort sind – also im Blut, im Lymphsystem, im peripheren Gewebe oder im Knochenmark. Die zentrale innere Uhr basiert auf einer Handvoll Gene, deren Ableseprodukte (die Proteine PER, CRY, REV-ERB, ROR, CLOCK und BMAL) wechselseitig ihre eigene Ablesung ein- und ausschalten. Ohne äußere Impulse oszilliert diese Rückkopplung mit einer Periode von etwas mehr als 24 Stunden. Durch Tageslichtsignale – von Nervenzellen in der Netzhaut an den Hypothalamus übermittelt – wird sie auf genau 24 Stunden eingestellt.
Die zentrale Uhrzeit wird vor allem durch das Zirbeldrüsen-Hormon Melatonin an die Zellen im gesamten Körper übermittelt. Die Melatoninkonzentration ist mitten in der Nacht am höchsten, fällt noch in der Nacht steil ab und bleibt tags sehr niedrig, bis sie abends wieder anzusteigen beginnt:
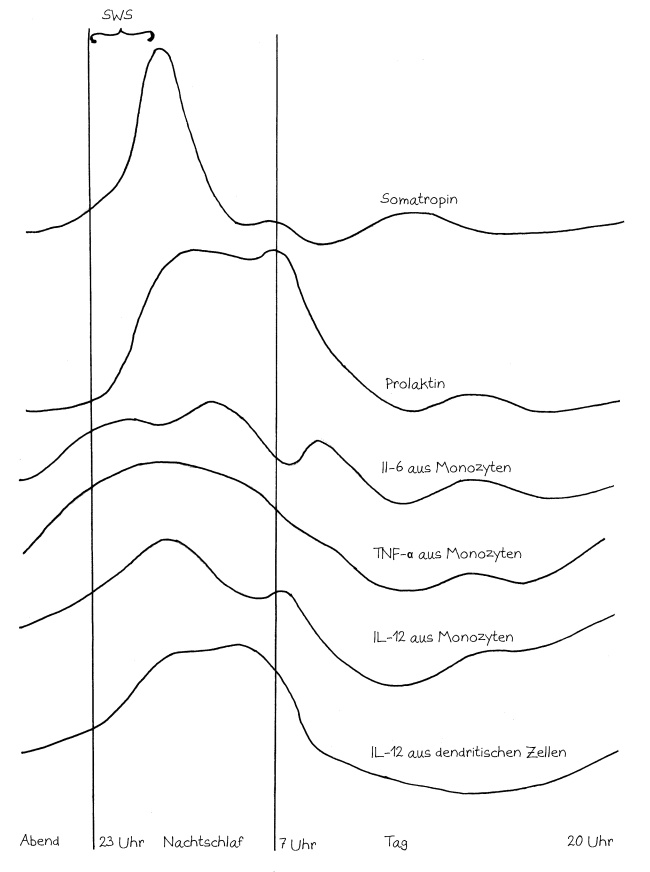
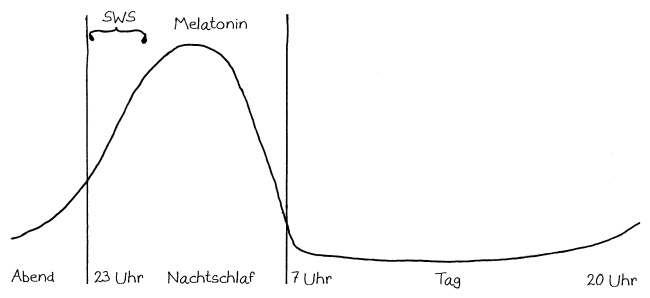 In dieser und den folgenden Abbildungen ist die Konzentration im Blut während etwas mehr als 24 Stunden dargestellt, beginnend mit dem Abend eines Tages bis zum Abend des nächsten Tages. Die beiden senkrechten Linien markieren die Nacht, in der man idealerweise zwischen 23 und 7 Uhr schläft. In der ersten Nachthälfte gerät man in den Tiefschlaf, hier wegen der englischen Bezeichnung slow-wave sleep als SWS bezeichnet. Diese Schlafphase ist für die Regelung des Immunsystems entscheidend.
In dieser und den folgenden Abbildungen ist die Konzentration im Blut während etwas mehr als 24 Stunden dargestellt, beginnend mit dem Abend eines Tages bis zum Abend des nächsten Tages. Die beiden senkrechten Linien markieren die Nacht, in der man idealerweise zwischen 23 und 7 Uhr schläft. In der ersten Nachthälfte gerät man in den Tiefschlaf, hier wegen der englischen Bezeichnung slow-wave sleep als SWS bezeichnet. Diese Schlafphase ist für die Regelung des Immunsystems entscheidend.
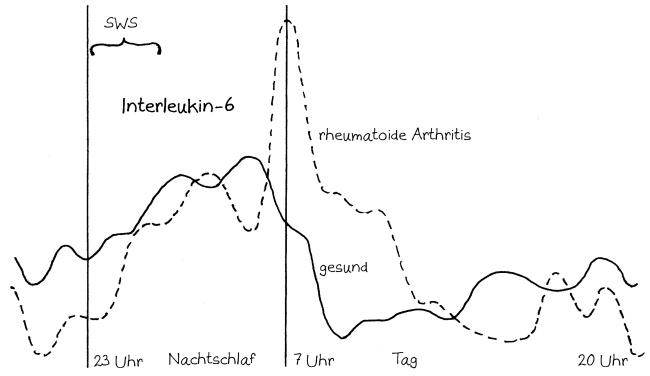
Vom Tiefschlaf gehen entzündungsfördernde Impulse an das Immunsystem aus, z. B. das Protohormon Somatropin, auch Wachstumshormon genannt, und das Hormon Prolaktin, die beide in der Hypophyse hergestellt werden. Werden die für diese Signale empfänglichen Immunzellen durch Antigene (z. B. Lipopolysaccharide aus Bakterien) aktiviert, so wandern sie nun von ihren Entstehungsorten und Ruheplätzen (v. a. dem Knochenmark) in das Blut und das Lymphsystem und produzieren große Mengen an entzündungsfördernden Zytokinen wie Interleukin-6 (IL-6), Interleukin-12 (IL-12) und Tumornekrosefaktor alpha (TNF-α). Morgens gehen die Zytokinproduktion und damit auch Entzündungsanzeichen wie Schwellungen zurück, sodass man sich tagsüber trotz Infektion gut fortbewegen kann:
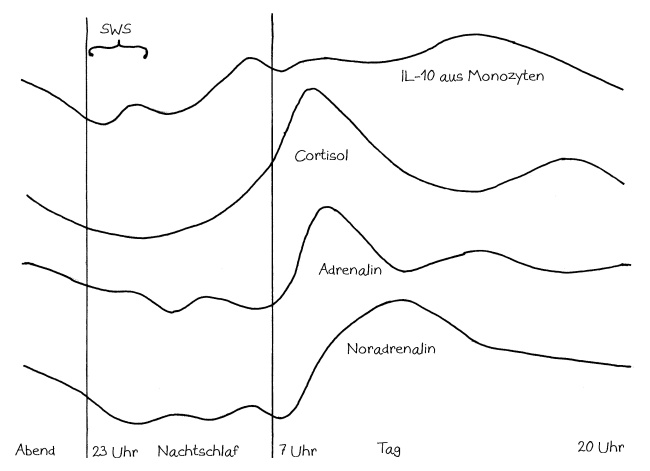
Zugleich wird nachts die Produktion des entzündungshemmenden Glukokortikiods Cortisol und der Katecholamine Adrenalin und Noradrenalin in der Nebennierenrinde durch die Tiefschlafsignale auf ein Minimum reduziert, ebenso die Herstellung entzündungshemmender Zytokine wie Interleukin-10 (IL-10) durch die Monozyten. Tags unterstützen diese entzündungshemmenden Substanzen dagegen die Wiederherstellung der Beweglichkeit und Handlungsfähigkeit:
Das heißt nun nicht, dass das Immunsystem tagsüber neue Bedrohungen wie plötzlich auftretende Antigene ignorieren würde. Vielmehr steigt die Produktion entzündungsfördernder Zytokine wie TNF-α in einem solchen Fall schnell an; in der Folge steigt dann auch die Konzentration des entzündungshemmenden Cortisols im Blut (gestrichelte Kurven). Beides wird binnen weniger Stunden wieder auf das Normalmaß heruntergeregelt, um den Tag-Nacht-Rhythmus nicht zu stören (sog. reaktive Homöostase):
Morgens erreicht neben der Cortisol- auch die Adrenalinproduktion ihren Höhepunkt. Adrenalin beeinflusst das Wanderungsverhalten zytotoxischer T-Zellen, die die Nacht über im Gewebe geruht haben und nun in die Blutbahn zurückkehren. So können sie tagsüber, wenn die Infektionsgefahr wegen unserer Aktivität am größten ist, Pathogene und kranke Zellen aus dem Weg räumen:
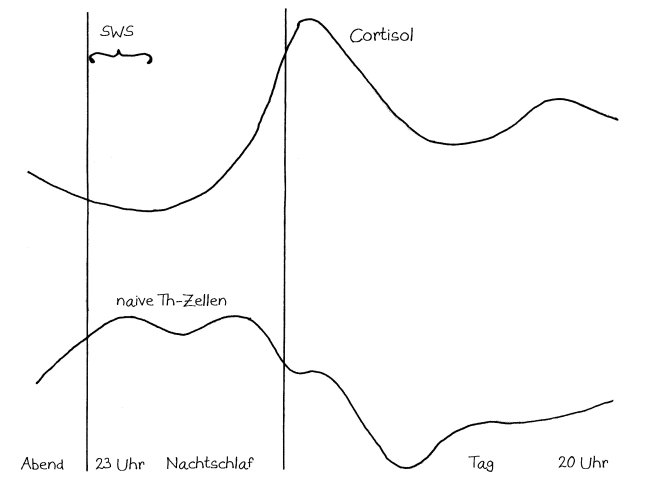
Der morgendliche Cortisol-Peak bringt dagegen „nachtaktive“ Immunzellen wie die T-Helferzellen (Th-Zellen) dazu, nun dem Ruf bestimmter Lockstoffe zu folgen und aus dem Blut und der Lymphe in das Knochenmark auswandern, wo sie gewissermaßen den Tag verschlafen:
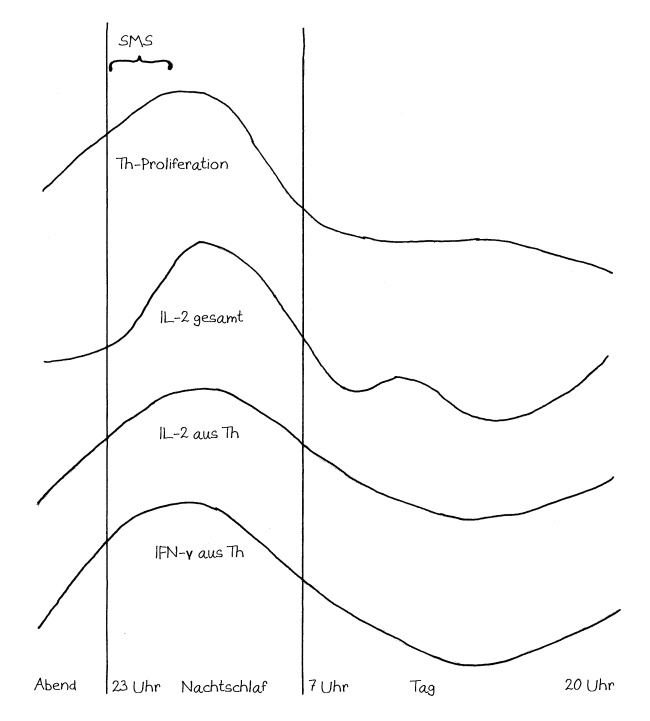
Wenn zu Beginn der Nacht kaum noch Cortisol durch den Körper kreist, verlassen die T-Helferzellen das Knochenmark wieder. Sie wandern in die Lymphknoten und lassen sich dort von antigenpräsentierenden Zellen die Antigen-Ausbeute vom letzten Tag präsentieren. Daraufhin vermehren sich diejenigen T-Helferzellen, die diese Antigene erkennen. Es entstehen vor allem T-Helferzellen vom Typ 1 (Th1), die den zellulären Arm der erworbenen Abwehr unterstützen. Ihre Aktivierung und Vermehrung begleiten sie mit der Produktion entsprechender Zytokine wie Interleukin-2 (IL-2) und Gamma-Interferon (IFN-γ):
Die Th1-Zellen unterstützen dann zum Beispiel B-Zellen bei der Produktion von opsonierenden Antikörpern, also Immunglobulinen des Typs IgG, die an Pathogene binden und sie damit für die Vernichtung durch Fresszellen markieren. Zugleich entstehen nachts Gedächtniszellen, sodass das Immunsystem bei einer erneuten Attacke derselben Pathogene schneller reagieren kann. Diese Umwandlung flüchtiger Information in dauerhafte Erinnerungen durch die Datenübertragung von den kurzlebigen antigenpräsentierenden Zellen auf langlebige T- und B-Gedächtniszellen dürfte eine der wichtigsten Funktionen unserer Nachtruhe sein.
Die gedächtnisbildenden und die unmittelbar gegen Pathogene wirksamen T-Zellen arbeiten also in unterschiedlichen Schichten, um sich nicht ins Gehege zu kommen.
Und was hat das alles mit Autoimmunerkrankungen zu tun? Offenbar ist bei einigen dieser chronischen Erkrankungen der Schichtplan gestört. Schon lange ist bekannt, dass Menschen mit rheumatoider Arthritis vor allem morgens unter Schmerzen und Gelenksteife leiden. Offenbar werden bei ihnen die nächtlichen Entzündungsreaktionen nicht rechtzeitig heruntergeregelt. Vor allem der Verlauf der Interleukin-6-Produktion ist gestört; sie erreicht etwa um 7 Uhr einen sehr hohen Gipfel und ist auch vormittags noch viel zu hoch: