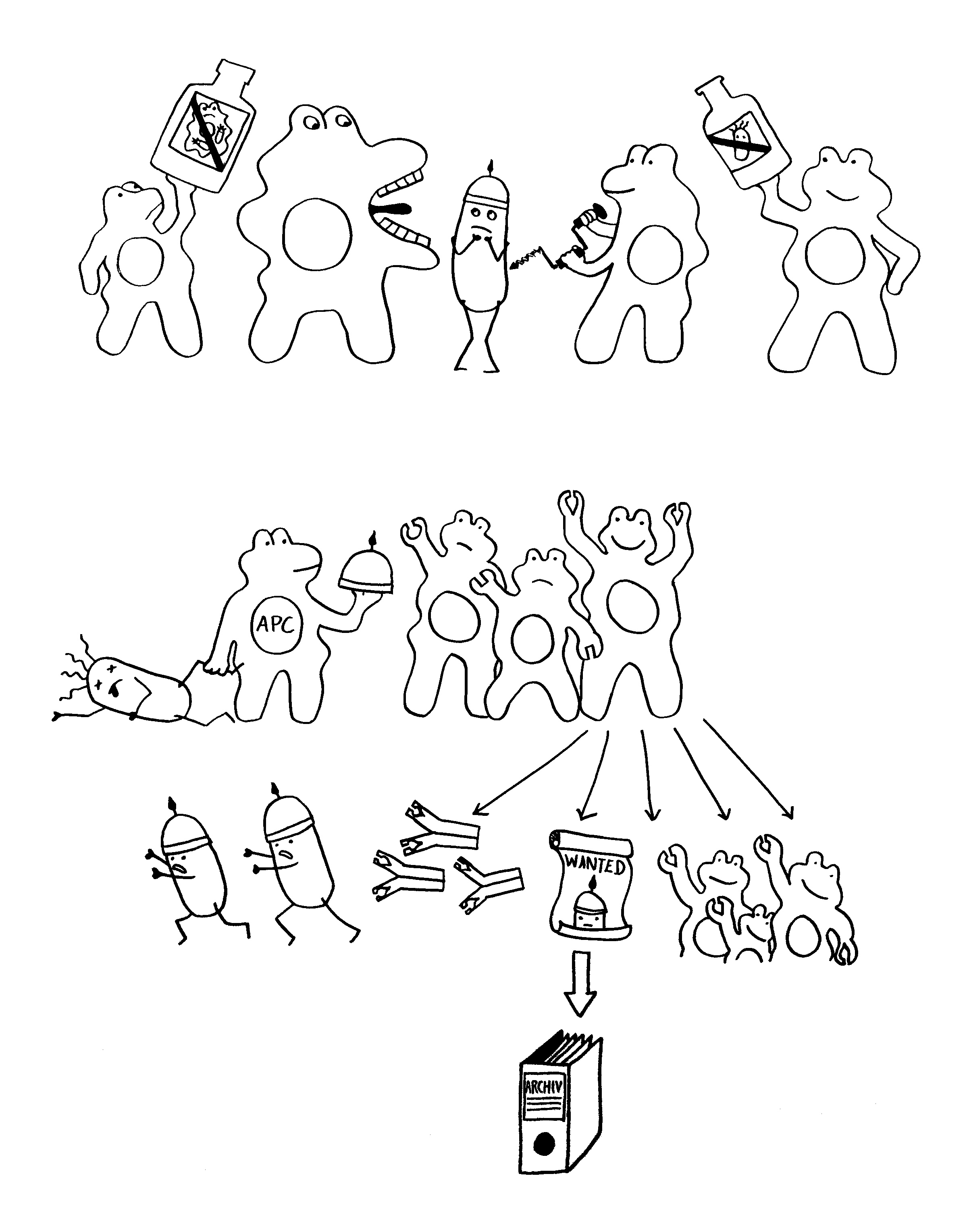
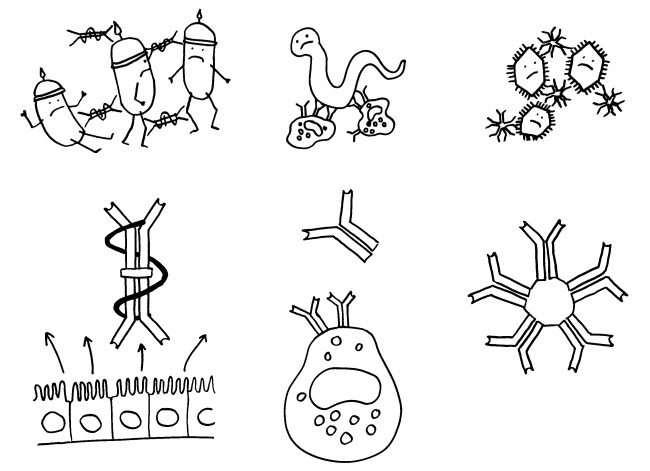
Vor gut 10 Jahren habe ich hier die Funktionsweise von CRISPR-Cas erklärt, dem erworbenen oder adaptiven Immunsystem der Bakterien und Archäen. Schon damals war bekannt, dass Prokaryoten-Zellen beim versehentlichen Einbau von Sequenzen aus dem eigenen Erbgut anstelle von Viren-Sequenzen an Autoimmunreaktionen sterben können. Und schon damals wurde die Frage gestellt, ob der Einbau eigener Sequenzen nicht auch andere Folgen, ja regelrechte Funktionen haben kann, etwa die Regulierung der Ablesung eigener Gene.
Heute ist in nature microbiology eine Arbeit erschienen, in der dies am Beispiel des Typ-IV-CRISPR-Cas-Systems des Bakteriums Pseudomonas oleovorans nachgewiesen wird. Der Artikel steckt hinter einer Bezahlschranke, aber das Manuskript ist an anderer Stelle frei zugänglich. Die Funktion der Typ-IV-Systeme waren der Forschung lange ein Rätsel, denn sie können fremde Nukleinsäuren, also virale Eindringlinge gar nicht zerschneiden. Nun zeigt sich, dass die spezifischen Erkennungssequenzen an bakterieneigene Gene binden und so deren Transkription unterdrücken – siehe Pressemitteilung beim idw.
Einen guten Überblick über die Vielfalt möglicher CRISPR-Cas-Funktionen jenseits der erworbenen Viren-Abwehr bietet eine frei zugängliche und mit anschaulichen Schemazeichnungen ausgestattete Übersichtsarbeit von Devi et al. (2022): CRISPR-Cas systems: role in cellular processes beyond adaptive immunity.