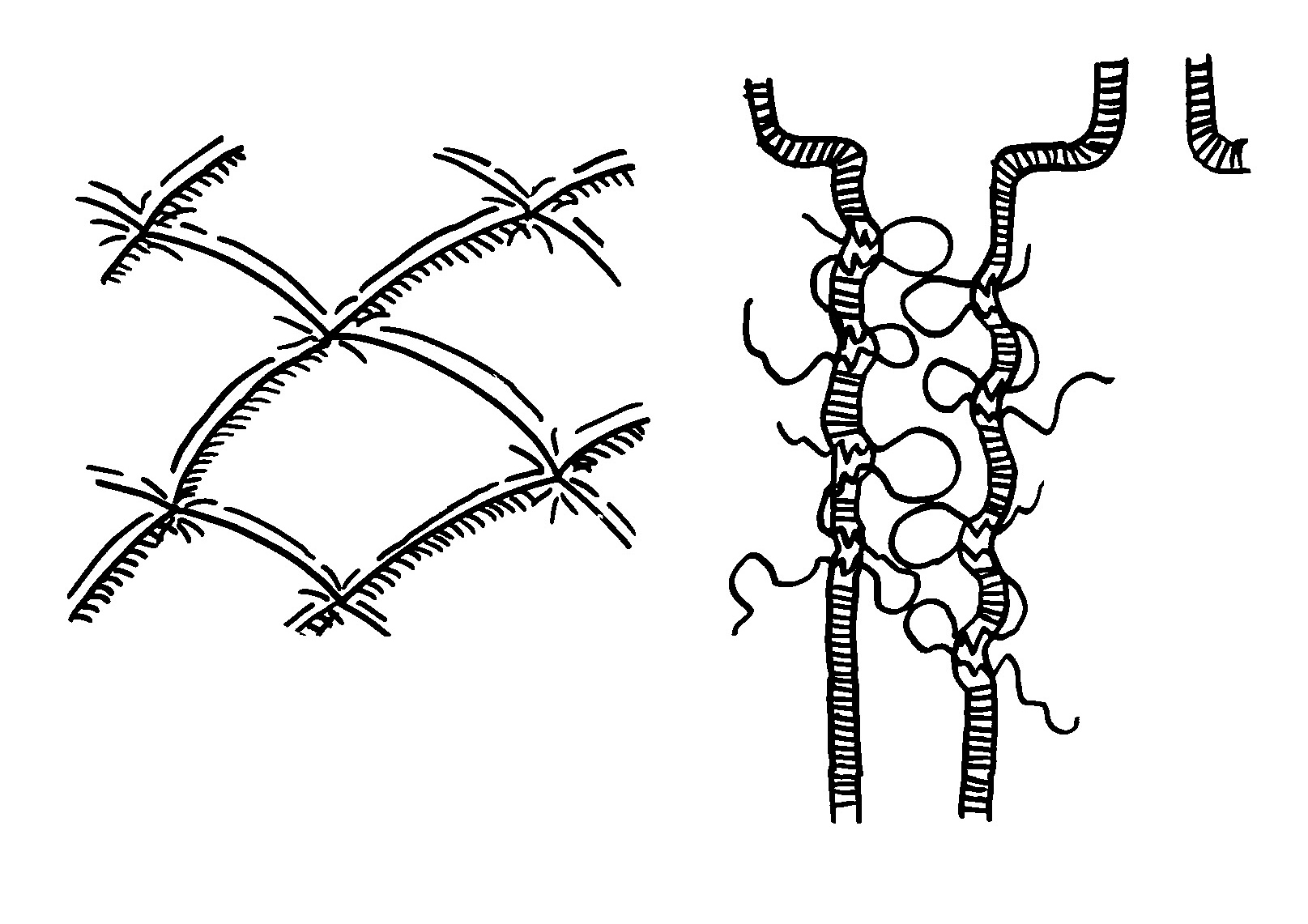
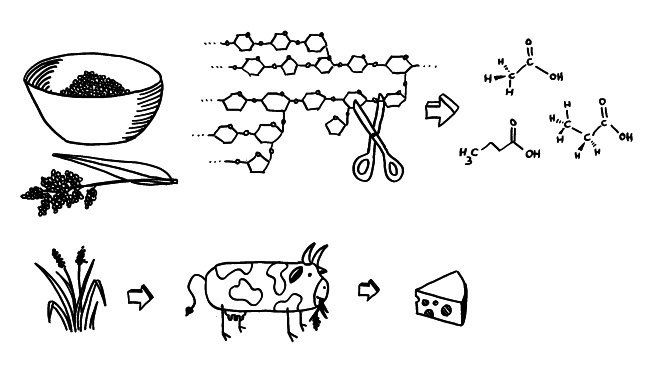
Nach langer Pause wegen Überstunden und Krankheit stürze ich mich wieder in die Arbeit am Buch. Ich bin immer noch mit der Beschreibung der wichtigsten Mechanismen beschäftigt, über die Infektionen mutmaßlich Autoimmunerkrankungen auslösen: molekulare Mimikry, Bystander Activation, Epitope Spreading und polyklonale Aktivierung, z. B. durch Superantigene.
Nebenbei wühle ich mich durch die Wissenschafts-Newsletter der letzten Monate. Evtl. fürs Buch relevante Meldungen verlinke ich hier. Den Anfang macht The Scientist, vor allem mit Meldungen zum Mikrobiom.
Microbes Fight Chronic Infection: Eine am 23.10.2014 in Nature veröffentlichte Studie zeigt, dass Clostridium scindens und in geringerem Umfang 10 weitere Bakterien-Taxa aus dem Darm-Mikrobiom Antibiotika-behandelte (und daher dysbiotische) Mäuse vor Infektionen mit Clostridium difficile schützen können. Evtl. lässt sich daraus eine Therapie für dysbiotische Menschen entwickeln, die weniger riskant ist als die Stuhltransplantationen, die derzeit in, äh, aller Munde sind.
Gut Microbes Trigger Malaria-Fighting Antibodies: Eine am 04.12.2014 in Cell veröffentlichte Studie zeigt, dass E. coli im Darm von Mäusen die Bildung von Antikörpern gegen den Kohlenwasserstoff Galα1-3Galb1-4GlcNAc-R (kurz: α-gal) auslöst, der sowohl an der Oberfläche der Bakterien als auch auf Malaria-Erregern (bei Mäusen Plasmodium berghei, bei Menschen Plasmodium falciparum) zu finden ist. Diese Antikörper sind auch im Blut gesunder Menschen in großen Mengen anzutreffen. Dank einer Dreifach-Mutation in den gemeinsamen Vorfahren der Menschen und der Menschenaffen stellen unsere Zellen kein α-gal mehr her, sodass die Antikörper nicht den eigenen Körper angreifen. Mit P. berghei infizierte Mäuse mit den durch das Bakterium induzierten Antikörpern im Blut erkrankten nur halb so häufig an Malaria wie Mäuse ohne die Antikörper. Weiterlesen →