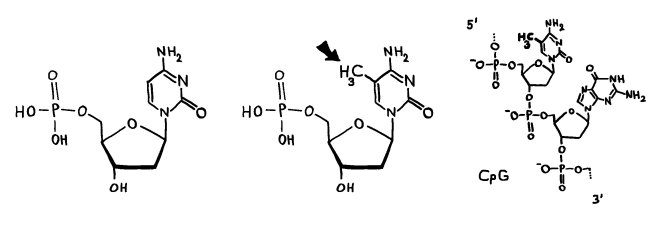
Zwei weitere Zeichnungen für den Einführungsteil des Buches: epigenetische Modifikation der DNA (Cytosin-Methylierung, oben) und der Histone (z. B. Serin-Phosphorylierung und Lysin-Acetylierung, unten).
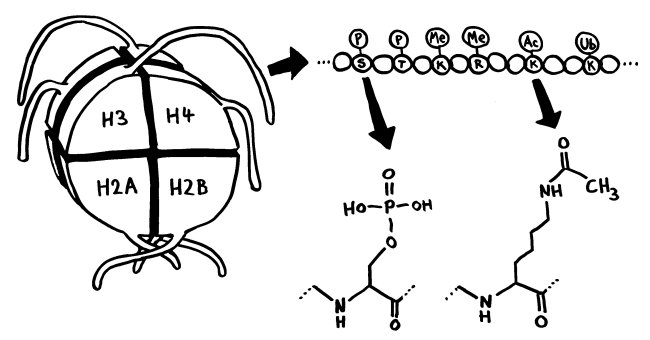 Ein Nukleosom besteht aus je zwei H2A-, H2B-, H3- und H4-Histonen, wobei die Scheibe von beiden Seiten gleich aussieht (d. h. hinter dem vorderen H3 steckt ein H4 usw.). Die DNA, die in den Chromosomen als linksgängige Superhelix gut anderthalb Mal um das Nukleosom gewunden ist, ist hier nicht dargestellt.
Ein Nukleosom besteht aus je zwei H2A-, H2B-, H3- und H4-Histonen, wobei die Scheibe von beiden Seiten gleich aussieht (d. h. hinter dem vorderen H3 steckt ein H4 usw.). Die DNA, die in den Chromosomen als linksgängige Superhelix gut anderthalb Mal um das Nukleosom gewunden ist, ist hier nicht dargestellt.
Der N-Schwanz des H3 ist am längsten und weist die meisten Phosphorylierungs- (P), Methylierungs- (Me), Acetylierungs- (Ac) und Ubiquitinierungsstellen (Ub) auf.
Quelle für den unteren rechten Teil: J Füllgrabe, N Hajji and B Joseph (2010): Cracking the death code: apoptosis-related histone modifications, Abb. 1

