Im Manuskript für den 2. Band stelle ich gerade dar, wie das Leben schwimmen lernte. LUCA, der letzte gemeinsame Urahn aller Lebensformen, hatte zwar vermutlich schon die Komplexität heutiger Bakterien und verfügte über ein ausgefeiltes Immunsystem (sogar mit einer erworbenen Abwehr, also einem Gedächtnis für frühere Infektionen). Aber er konnte sich wohl noch nicht fortbewegen und war daher an jenen hydrothermalen Schlot am Meeresgrund oder einen ähnlichen Ort gebunden, an dem er aus präbiotischen Makromolekülen entstanden war.
Sowohl Archaeen als auch Bakterien, die beiden Hauptäste des Stammbaums allen Lebens, können sich mit rotierenden Zellanhängen durchs Wasser schrauben, aber kurioserweise sind diese ähnlich funktionierenden Anhänge komplett unterschiedlich konstruiert, was auf eine Entstehung erst nach der ersten Aufspaltung des Lebensbaums hinweist. Beide Apparaturen, die Flagellen der Bakterien und die Archaellen der Archaeen, sind zudem unglaublich kompliziert aufgebaut, und sie scheinen vom Himmel gefallen zu sein: Man kennt keine einfacheren Vorformen.
Solche Fälle von „irreduzibler Komplexität“ werden von Kreationisten gerne als Belege für intelligent design angeführt, also für das zielgerichtete, planmäßige Wirken eines Schöpfers. Aber das ist Unsinn. Vielmehr geht eine solche irreduzible Komplexität auf ein Grundprinzip der darwinistischen Evolution zurück: die Exaptation, die „Zweckentfremdung“ bestehender Eigenschaften von Lebewesen.
Dieses Prinzip hat der Molekularbiologe François Jacob bereits in den frühen 1980ern in seinem Essay „Die Bastelei der Evolution“ dargestellt: „Die Evolution schafft ihre Neuheiten, anders als der Ingenieur, nicht aus dem Nichts. Sie arbeitet mit dem, was bereits vorhanden ist, sei es, daß sie ein älteres System abändert und ihm eine neue Funktion zuweist, sei es, daß sie mehrere Systeme zu einem komplexeren zusammenfaßt. […] kurz, wie ein Bastler, der das, was er um sich herum findet, benutzt, um daraus einen brauchbaren Gegenstand zu machen. […] Wenn aus einem Teil der Speiseröhre eine Lunge wird, dann ist das etwas ganz Ähnliches, wie wenn aus Omas Gardine ein Rock wird.“
Diese Wiederverwendung alter Strukturen in neuen Zusammenhängen führt zwangläufig dazu, dass die so entstandenen Organe oder Zellstrukturen teils unlogisch wirken und teils irreduzibel komplex: Sie tragen ihre gesamte Entstehungsgeschichte mit sich herum, ihre Anpassung an die ehemalige Funktion. Ihre weitere Entwicklung verläuft in vorgebahnten, tief ausgewaschenen Tälern der Evolutionslandschaft. Sie haben wilde Steampunk-Schnörkel und arbeiten mit zehn Zahnrädern, wo ein Ingenieur sich auf zwei beschränken würde.
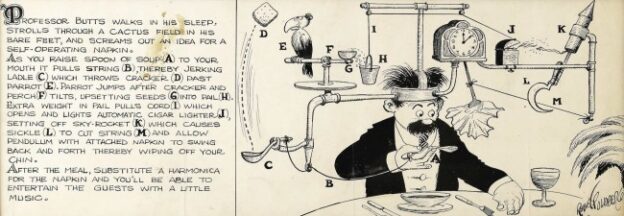
In einem Einführungsartikel zu einer Forschungsarbeit hat Morgan Beeby die Archaellen und mit ihnen verwandte fädige Zellanhänge bei den Archaeen und Bakterien 2019 mit den allseits beliebten Rube-Goldberg-Maschinen verglichen: Die Proteingruppe, zu der sie gehören, die sogenannte TFF-Superfamilie, wurde im Lauf der Evolution zu einem abenteuerlichen Maschinenpark, in dem wir Injektionspumpen, Saugroboter, Enterhaken, rotierende Peitschen und allerlei andere Geräte finden. Alle gehen sie vermutlich auf einen ein- und ausfahrbaren Stab zurück, mit dem unser Urahn LUCA DNA aus seiner Umgebung eingesammelt hat.
Dieses Gefühl, eine unnötig komplizierte Maschinerie vor sich zu haben, kennen vermutlich alle, die sich mit dem menschlichen Immunsystem auseinandersetzen. Auch das lässt sich nur durch die Bastelei der Evolution erklären, die im ewigen Pingpong der Angriffe von Parasiten und der Abwehr seitens ihrer Wirte zu allem gegriffen hat, was sie finden konnte. Aus Streichhölzern und Gummibändern hat sie in gut vier Milliarden Jahren trojanische Pferde gebaut, die in trojanischen Pferden stecken, die in trojanischen Pferden stecken.
Literatur:
François Jacob: „Le jeu des possibles. Essai sur la diversité du vivant“, Fayard 1981. Zitat aus der deutschen Übersetzung von Friedrich Griese, Taschenbuch-Ausgabe 1984 unter dem Titel „Das Spiel der Möglichkeiten“ bei Piper; dort auf S. 50ff.
Morgan Beeby (2019): Evolution of a family of molecular Rube Goldberg contraptions