Hintergrund/Ergänzungen zum vorigen Artikel über eine Säugetier-Sialinsäure als Xenoautoantigen:
Ajit Varki, Pascal Gagneux: Human-specific evolution of sialic acid targets: Explaining the malignant malaria mystery? PNAS 106(35), 2009, 14739-14740
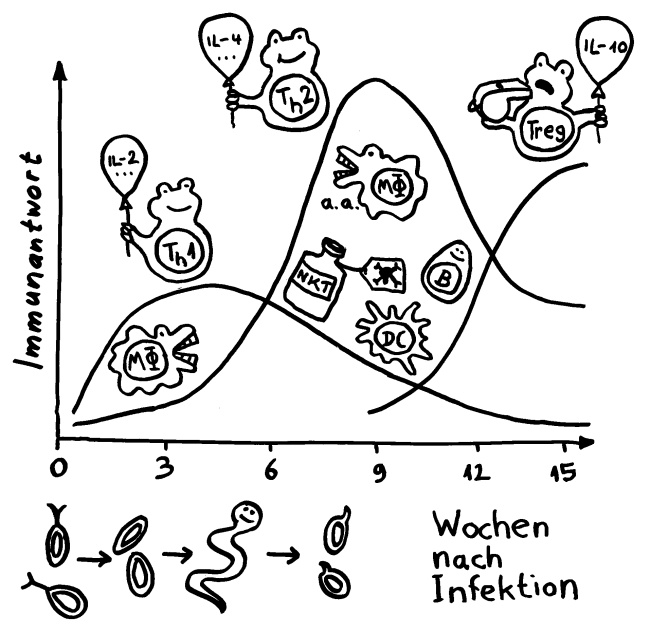
Plasmodium falciparum verursacht schwere Malaria beim Menschen; nächster Verwandter, P. reichenowi, infiziert Schimpansen und Gorillas, richtet bei ihnen aber weniger Schaden an. Übertragung P. falciparum durch Anopheles-Mücken. Nach Mückenstich infizieren die injizierten Sporozoiten Leberzellen -> Merozoiten, die in die zirkulierenden roten Blutkörperchen (RBCs) eindringen und deren zyklische asexuelle Vermehrung Schübe hohen Fiebers auslösen. P. falciparum exprimiert mehrere Bindungsproteine, die spezifische Ziele auf den RBCs erkennen – vor allem die Sialinsäuren an den Enden der Glykanketten an den Glycophorinen (den häufigsten Oberflächenglykoproteinen) der RBCs.
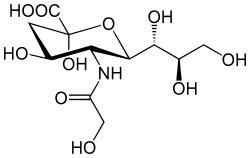
Das „Sialom“ oder Sialinsäure-Repertoire des Wirts muss sich ständig weiterentwickeln, da die Pathogene schnell evolvieren. Z. B. kam es vor etwa 2-3 Mio. Jahren zu einer Alu-vermittelten Deletion im CMAH-Gen unserer Vorfahren -> keine Biosynthese von Neu5Gc mehr, dafür Akkumulation des Ausgangsstoffes Neu5Ac. Bei den übrigen Menschenaffen kommen beide Sialinsäuren vor. Das wichtigste RBC-Bindungsprotein der Merozoiten von P. falciparum bindet bevorzugt Neu5Ac, das von P. reichenowi bevorzugt Neu5Gc. Der Verlust von Neu5Gc könnte unsere Vorfahren kurzfristig von schwerer Malaria befreit haben. Demnach wäre P. falciparum später entstanden, als das Erkennungsprotein EBA-175 so mutierte, dass es Neu5Ac auf den Erythrozyten erkannte. Vermutlich gab es ein Zwischenstadium, indem EBA-175 beide Formen binden konnte. Weiterlesen →
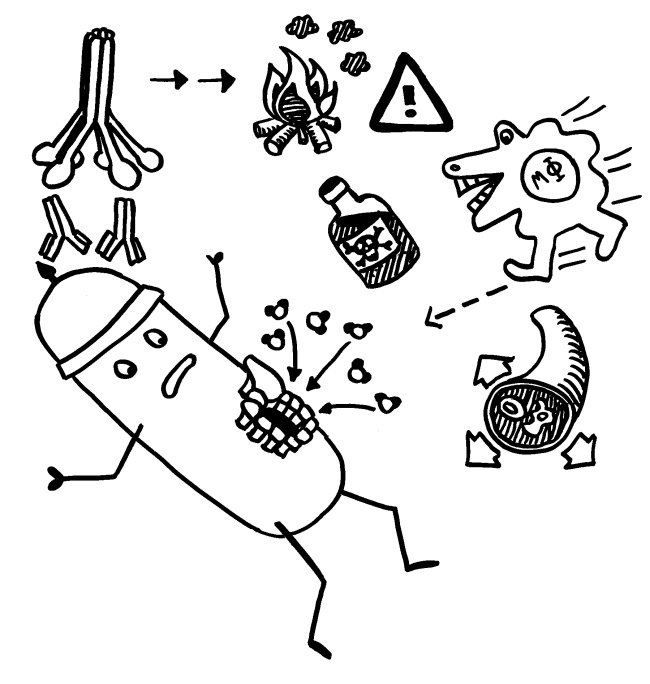 Das Protein C1 bindet an Antikörper, die wiederum an Antigene auf den Pathogenen binden, und löst Reaktionskaskaden aus. In deren Verlauf werden nicht nur die „Brunnenlöcher“ (Membranangriffskomplexe aus C9) gebohrt, sondern auch die kleinen Arterien weitgestellt (schnellerer Transport von Immunzellen zum Ort der Infektion), Histamin aus Mastzellen ausgeschüttet (Botenstoff in der Entzündungsreaktion) sowie Phagozyten (Fresszellen) durch Chemotaxis angelockt und durch die Opsonierung der Pathogene zu deren Verzehr angeregt. Das Komplementsystem gehört zur angeborenen Immunabwehr und wird von vielen Bakterien und Viren durch molekulare Mimikry und Blockaden ausgehebelt.
Das Protein C1 bindet an Antikörper, die wiederum an Antigene auf den Pathogenen binden, und löst Reaktionskaskaden aus. In deren Verlauf werden nicht nur die „Brunnenlöcher“ (Membranangriffskomplexe aus C9) gebohrt, sondern auch die kleinen Arterien weitgestellt (schnellerer Transport von Immunzellen zum Ort der Infektion), Histamin aus Mastzellen ausgeschüttet (Botenstoff in der Entzündungsreaktion) sowie Phagozyten (Fresszellen) durch Chemotaxis angelockt und durch die Opsonierung der Pathogene zu deren Verzehr angeregt. Das Komplementsystem gehört zur angeborenen Immunabwehr und wird von vielen Bakterien und Viren durch molekulare Mimikry und Blockaden ausgehebelt.