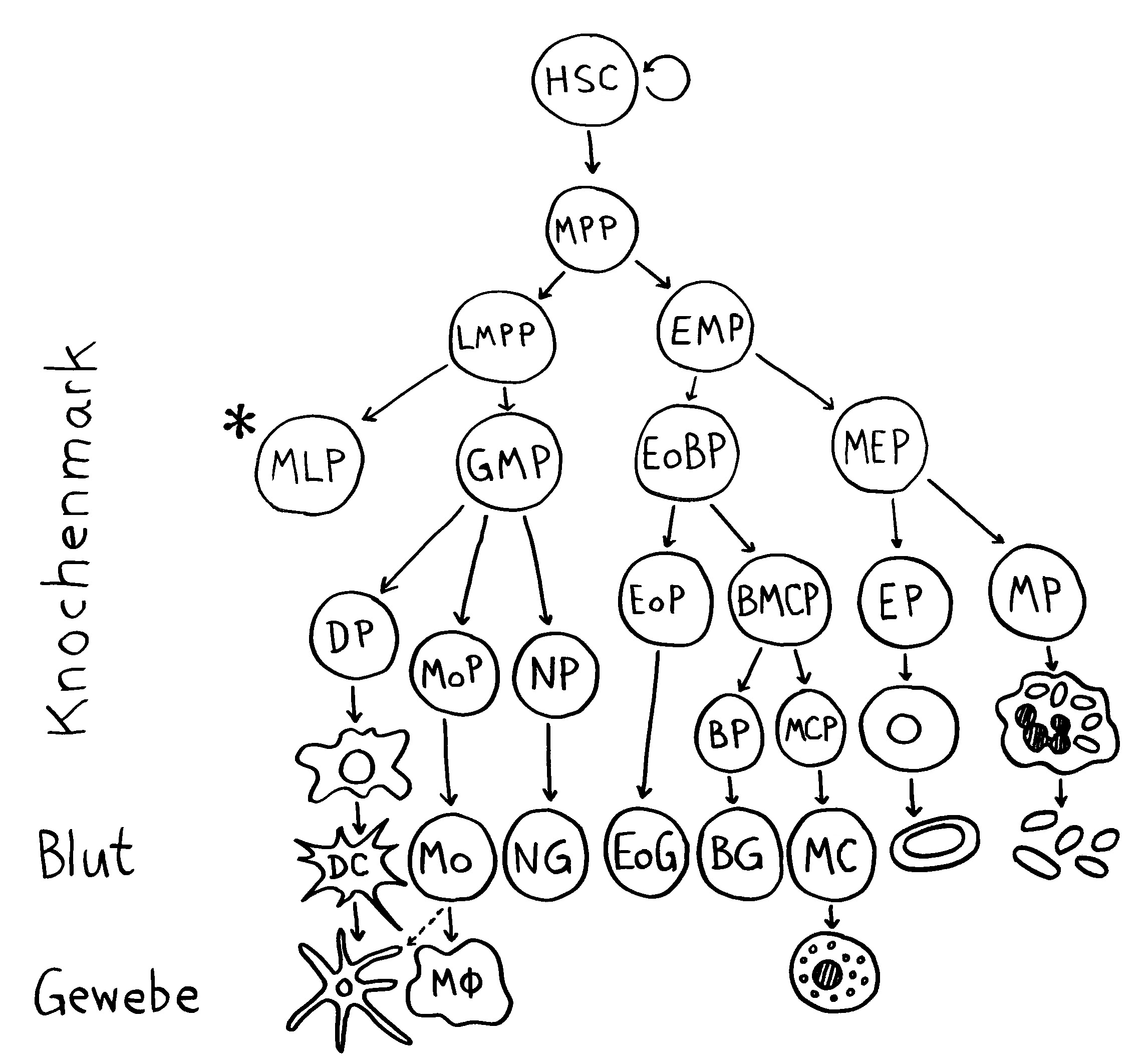
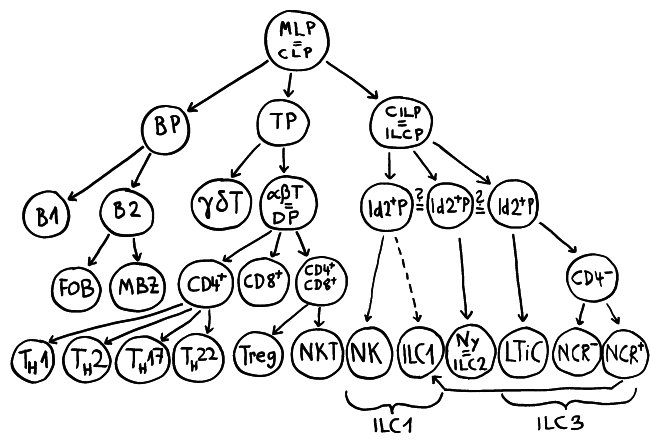
Der hämatopoetische Stammbaum zeigt, wie die Blutzellen miteinander verwandt sind. Alle gehen aus hämatopoetischen Stammzellen (HSC) hervor. Hier ist der myeloische Ast dargestellt. Die Entstehung der Lymphozyten und ihrer Verwandten aus dem multilineage progenitor (*) folgt in Abb. 120. Die fertigen Blutzellen sind unten in den Zeilen »Blut« und »Gewebe« aufgereiht. Rechts in der Blut-Reihe stehen die roten Blutkörperchen und die winzigen Blutplättchen, die beide nicht zu den Immunzellen zählen. Dendritische Zellen und Mastzellen findet man im Blut kaum, weil sie nach ihrer Entstehung gleich ins Gewebe einwandern. Makrophagen entstehen ohnehin erst im Gewebe, und zwar aus eingewanderten Monozyten.
Die neutrophilen Granulozyten (NG) sind offenbar nicht näher mit den eosinophilen Granulozyten (EoG) und den basophilen Granulozyten (BG) verwandt. Außerdem stehen die basophilen Granulozyten den Mastzellen (MC) näher als den eosinophilen Granulozyten. Die klassische Einteilung anhand des mikroskopischen Erscheinungsbilds (zahlreiche Vesikel oder »Körnchen« = granula in allen Granulozyten) führt also in die Irre.
V. o. n. u. und v. l. n. r.: HSC = hämatopoetische Stammzelle, MPP = multipotent progenitor, LMPP = lymphoid-primed multipotent progenitor, EMP = erythro-myeloid progenitor, MLP = multilineage progenitor, GMP = granulocyte/monocyte progenitor, EoBP = eosinophil/basophil progenitor, MEP = myeloid-erythroid progenitor, DP = dendritic cell progenitor, MoP = monocyte progenitor, NP = neutrophil progenitor, EoP = eosinophil progenitor, BMCP = basophil/mast cell progenitor, EP = erythrocyte progenitor, MP = megakaryocyte progenitor, BP = basophil progenitor, MCP = mast cell progenitor; DC = dendritische Zelle, Mo = Monozyt, NG = neutrophiler Granulozyt, EoG = eosinophiler Granulozyt, BG = basophiler Granulozyt, MC = Mastzelle, MΦ = Makrophage. Progenitor heißt Vorläufer.
Sie dürfen diese Zeichnung gerne in Folien etc. übernehmen, sofern Sie die Quelle angeben: Dr. Andrea Kamphuis, https://autoimmunbuch.de