 Weitere Skizzen für Teil III des Buches (Evolution des Immunsystems): In den letzten Jahren hat man bei Pflanzen Mutationen entdeckt, die offenbar die Pathogen-Abwehr verrücktspielen lassen. Selbst ohne Pathogen-Angriff werden Signalketten in Gang gesetzt, die zum Absterben von Gewebeteilen führen – was eigentlich die Ausbreitung von Pathogenen verhindern soll.
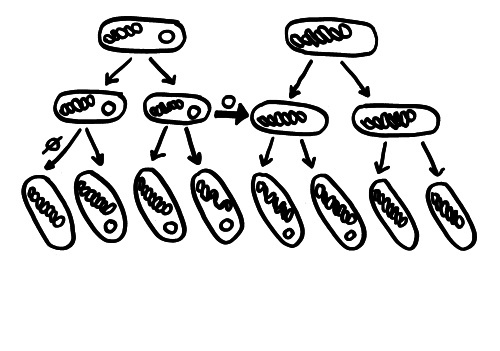
Weitere Skizzen für Teil III des Buches (Evolution des Immunsystems): In den letzten Jahren hat man bei Pflanzen Mutationen entdeckt, die offenbar die Pathogen-Abwehr verrücktspielen lassen. Selbst ohne Pathogen-Angriff werden Signalketten in Gang gesetzt, die zum Absterben von Gewebeteilen führen – was eigentlich die Ausbreitung von Pathogenen verhindern soll.
Andere Pflanzen können auch ohne Mutation überreagieren, wenn sich ihre Umwelt verändert: Gehölze, die die Invasion eines Borkenkäfers und eines mit ihm in Symbiose lebenden Pilzes spüren, versperren ihre Wassertransportwege (das Xylem) durch Callose, Lignin und ähnliche Substanzen, um die Ausbreitung des Pilzmyzels zu stoppen. Wenn exotische Käfer und Pilze zum Beispiel mit Holzpaletten in Frachtschiffen oder -flugzeugen auf einen neuen Kontinent gelangen, kann es einer aktuellen Hypothese zufolge zu fatalen „olfaktorischen Missverständnissen“ kommen:
 Die Käfer, die in ihrer Heimat nur an toten oder bereits sterbenden Bäume interessiert sind, befallen lebende Bäume, weil diese so ähnlich riechen wie daheim das tote Holz. Die Pilze tricksen die pflanzliche Abwehr zunächst so weit aus, dass sie große Teile des Xylems befallen können. Wenn der Baum diese Transportwege daraufhin verstopft, erwürgt er sich gewissermaßen selbst: Er vertrocknet, weil das Wasser aus dem Boden nicht mehr in die Krone gelangt. Das scheint z. B. bei dem Pilz Raffaelea lauricola und dem Käfer Xyleborus glabratus der Fall zu sein, die gemeinsam aus Asien nach Nordamerika gelangt sind und dort zum Beispiel ganze Avocado-Plantagen absterben lassen.
Die Käfer, die in ihrer Heimat nur an toten oder bereits sterbenden Bäume interessiert sind, befallen lebende Bäume, weil diese so ähnlich riechen wie daheim das tote Holz. Die Pilze tricksen die pflanzliche Abwehr zunächst so weit aus, dass sie große Teile des Xylems befallen können. Wenn der Baum diese Transportwege daraufhin verstopft, erwürgt er sich gewissermaßen selbst: Er vertrocknet, weil das Wasser aus dem Boden nicht mehr in die Krone gelangt. Das scheint z. B. bei dem Pilz Raffaelea lauricola und dem Käfer Xyleborus glabratus der Fall zu sein, die gemeinsam aus Asien nach Nordamerika gelangt sind und dort zum Beispiel ganze Avocado-Plantagen absterben lassen.
(Lit.: Jiri Hulcr & Robert R. Dunn, 2011, und andere Arbeiten auf dieser Literaturliste)