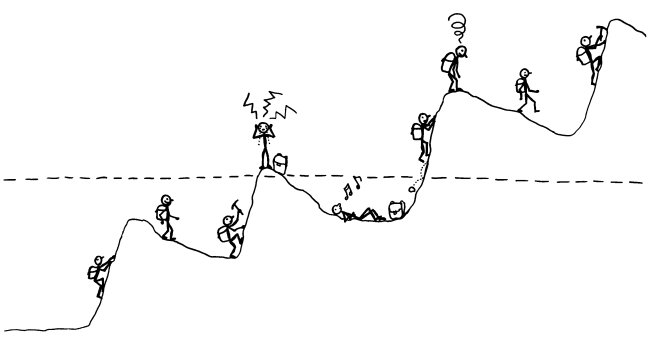
 Viele Autoimmunerkrankungen verlaufen schubförmig. Am bekanntesten ist das bei der schubförmig remittierenden Multiplen Sklerose (RR-MS). Aber auch bei Typ-1-Diabetes kann auf den ersten Ausbruch von Symptomen, der zur Diagnose führt, eine Zeit der scheinbaren Genesung folgen – die sogenannte Honeymoon-Phase. Und bei den meisten Autoimmunerkrankungen geht der symptomatischen Phase (oberhalb der gestrichelten Linie) unbemerkt eine langjährige Entgleisung des Immunsystems voran, bei der nach und nach mehr Autoantikörper oder autoreaktive T-Zellen entstehen und es den regulatorischen T-Zellen immer schwerer fällt, diese selbstzerstörerischen Elemente in den Griff zu bekommen.
Viele Autoimmunerkrankungen verlaufen schubförmig. Am bekanntesten ist das bei der schubförmig remittierenden Multiplen Sklerose (RR-MS). Aber auch bei Typ-1-Diabetes kann auf den ersten Ausbruch von Symptomen, der zur Diagnose führt, eine Zeit der scheinbaren Genesung folgen – die sogenannte Honeymoon-Phase. Und bei den meisten Autoimmunerkrankungen geht der symptomatischen Phase (oberhalb der gestrichelten Linie) unbemerkt eine langjährige Entgleisung des Immunsystems voran, bei der nach und nach mehr Autoantikörper oder autoreaktive T-Zellen entstehen und es den regulatorischen T-Zellen immer schwerer fällt, diese selbstzerstörerischen Elemente in den Griff zu bekommen.
Schlagwort-Archiv: Tregs
Neue Literatur bis einschließlich Dezember 2013, Teil 4
Der Rest, wieder unkommentiert und noch nicht verschlagwortet:
Matarese G et al. (2013): Hunger-promoting hypothalamic neurons modulate effector and regulatory T-cell responses (Open Access) T3
Dazu auch Neurons Govern Immunity: Hunger-associated molecules in the hypothalamus suppress inflammation.
Yu X et al. (2013): TH17 Cell Differentiation Is Regulated by the Circadian Clock (Abstract; PDF aber an anderer Stelle erhältlich) T3, T4
Dazu auch Time for T cells: Circadian rhythms control the development of inflammatory T cells, while jet lag sends their production into overdrive.
Scher JU et al. (29139: Expansion of intestinal Prevotella copri correlates with enhanced susceptibility to arthritis (Open Access) T4
Dazu auch Gut Microbes May Impact Autoimmunity: Researchers show that the prevalence of one genus of bacteria correlates with the onset of rheumatoid arthritis.
Zhong W et al. (2013): Immune anticipation of mating in Drosophila: Turandot M promotes immunity against sexually transmitted fungal infections (Open Access) T4
Dazu auch Frisky Fruit Flies: Researchers show that Drosophila females upregulate an immune gene for protection against sexually transmitted infections before copulation.
Simmonds MJ et al. (2013): Skewed X chromosome inactivation and female preponderance in autoimmune thyroid disease: an association study and meta-analysis (Abstract) T4
Alexandraki KI et al. (2013): Are patients with autoimmune thyroid disease and autoimmune gastritis at risk of gastric neuroendocrine neoplasms type 1? (Abstract) T3
Leskela S et al. (2013) Plasmacytoid Dendritic Cells in Patients With Autoimmune Thyroid Disease (Abstract) T3
Ioannou M et al. (2013): In Vivo Ablation of Plasmacytoid Dendritic Cells Inhibits Autoimmunity through Expansion of Myeloid-Derived Suppressor Cells (Open Access) T3
Simmonds MJ et al. (2013): GWAS in autoimmune thyroid disease: redefining our understanding of pathogenesis (Abstract) T3
Rege S, Hodgkinson SJ (2013): Immune dysregulation and autoimmunity in bipolar disorder: Synthesis of the evidence and its clinical application (Abstract) T3?
Abwehrreihen
Neue Skizze fürs Buch:
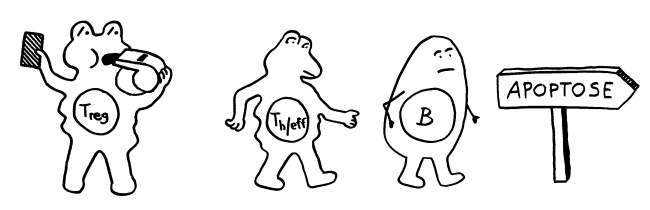
 Die Zellen des Immunsystems stellen sich in mehreren Abwehrreihen auf. Vorn stehen Zellen der angeborenen Immunität wie Mastzellen, dendritische Zellen und Makrophagen, im Mittelfeld die unterschiedlichen Granulozyten und in der letzten Verteidigungsreihe zytotoxische T-Zellen, T-Helferzellen, natürliche Killer-T-Zellen und ILCs. Der Torwart ist eine Plasmazelle (B-Zelle). Regulatorische T-Zellen (Tregs) pfeifen das Spiel rechtzeitig ab.
Die Zellen des Immunsystems stellen sich in mehreren Abwehrreihen auf. Vorn stehen Zellen der angeborenen Immunität wie Mastzellen, dendritische Zellen und Makrophagen, im Mittelfeld die unterschiedlichen Granulozyten und in der letzten Verteidigungsreihe zytotoxische T-Zellen, T-Helferzellen, natürliche Killer-T-Zellen und ILCs. Der Torwart ist eine Plasmazelle (B-Zelle). Regulatorische T-Zellen (Tregs) pfeifen das Spiel rechtzeitig ab.
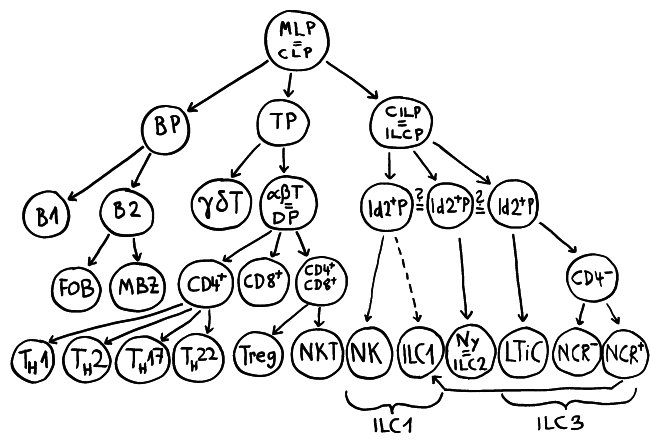
Reformierter Immunzellstammbaum, Teil 2
Überblick: Typ-1-Diabetes
Diese Review-Sammlung der Zeitschrift Cold Spring Harbor Perspectives in Medicine umfasst 18 frei zugängliche Artikel aus dem Jahr 2012, von denen ich bisher fünf gelesen habe. Notizen zum Einführungsartikel:
Mark A. Atkinson, Pathogenese und Naturgeschichte von T1D: sehr guter Überblick, auch über ungeklärte Fragen.
Anteil T1D-Fälle, die erst bei Erwachsenen diagnostiziert werden: 35-50%. Etwa 5-15% der Erwachsenen mit T2D-Diagnose dürften tatsächlich T1D haben. 2 Gipfel: erster bei Kindern von 5-7 Jahren, zweiter nahe Pubertät. M und F etwa gleich oft betroffen, leichter Männerüberschuss. T1D-Diagosen im Herbst und Winter häufiger als im Frühjahr/Sommer -> evtl. Umweltfaktor an Symptomausbruch beteiligt. Studie SEARCH: Etwa 0,26% aller unter 20-Jährigen haben Diabetes (T1D oder T2D); bei unter 10-Jährigen 19,7/100.000 neue Fälle/Jahr, bei über 10-Jährigen 18,6/100.000; Ethnien: bei weißen Nicht-Latinos unter 10 Jahren höchste Inzidenz (24,8/100.000).
Bandbreite der Inzidenzen zwischen Ländern, aus denen Daten vorliegen: über 350-fach! I. A. positiv korreliert mit Breitengrad. Selten in Indien, China, Venezuela; sehr häufig in Finnland (> 60/100.000/Jahr) und Sardinien (etwa 40/100.000/Jahr); > 20/100.000/Jahr in Schweden, Norwegen, Portugal, GB, Kanada, Neuseeland. Estland: weniger als 75 Meilen von Finnland entfernt, aber T1D-Rate weniger als 1/3 der finnischen. Puerto Rico: selbe Rate wie Festland-USA, benachbartes Kuba dagegen weniger als 3/100.000/Jahr. Inzidenzen steigen weltweit seit Jahrzehnten, besonders stark bei den unter 5-Jährigen. In Schweden scheint Plateau erreicht zu sein. Anstieg viel zu schnell für Verschiebung der genetischen Empfänglichkeit. Anteil Betroffener mit Risikoallelen (v. a. im MHC-II-Komplex) scheint vielmehr gesunken zu sein. Weiterlesen
Was passiert bei Immunneuropathien?
Ich habe meine Fazialislähmung zum Anlass genommen, für das Buch zu skizzieren, wie eine Immunneuropathie abläuft. Zu den Immunneuropathien zählen Autoimmunerkrankungen wie Multiple Sklerose, das Guillain-Barré-Syndrom, chronisch inflammatorische demyelinisierende Polyneuropathie (CIDP) oder vaskulitische Neuropathie. Bei einigen ist das periphere, bei anderen das zentrale Nervensystem betroffen. Oft beschränkt sich die Störung (wie bei der Fazialislähmung) auf einen einzelnen Nerv.
Am Anfang steht vermutlich immer die Reaktivierung eines latenten Virus (z. B. Herpes) oder eine oftmals unbemerkte, da symptomfreie (sogenannte stumme oder maskierte) Infektion, hier durch ein maskiertes Bakterium dargestellt. Eine in der Blutbahn oder im Gewebe patrouillierende Immunzelle – hier eine dendritische Zelle (DC) – entdeckt den Eindringling:
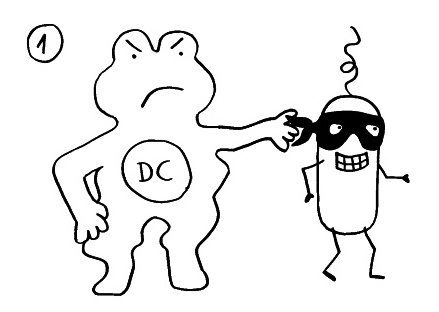 Die dendritische Zelle nimmt Teile des Erregers auf und verarbeitet sie zu einem präsentablen Antigen weiter. Sie verwandelt sich in eine antigenpräsentierende Zelle (APC), die einer T-Helferzelle das Antigen auf ihrem MHC-Klasse-II-Rezeptor (hier: Tablett) präsentiert. Damit es nicht zu Fehlalarmen kommt, gibt es einen Sicherheitsmechanismus: T-Helferzellen reagieren nur dann auf ein Antigen, wenn ihnen gleichzeitig auf einem anderen Rezeptor ein sogenanntes kostimulierendes Signal präsentiert wird, das anzeigt, dass wirklich eine Infektion oder eine andere Gefahr vorliegt, die bekämpft werden muss (hier: Kerze). Auf der Oberfläche der T-Zelle gibt es für beide Signale spezifische Rezeptoren (hier: Augen/Blickkontakt):
Die dendritische Zelle nimmt Teile des Erregers auf und verarbeitet sie zu einem präsentablen Antigen weiter. Sie verwandelt sich in eine antigenpräsentierende Zelle (APC), die einer T-Helferzelle das Antigen auf ihrem MHC-Klasse-II-Rezeptor (hier: Tablett) präsentiert. Damit es nicht zu Fehlalarmen kommt, gibt es einen Sicherheitsmechanismus: T-Helferzellen reagieren nur dann auf ein Antigen, wenn ihnen gleichzeitig auf einem anderen Rezeptor ein sogenanntes kostimulierendes Signal präsentiert wird, das anzeigt, dass wirklich eine Infektion oder eine andere Gefahr vorliegt, die bekämpft werden muss (hier: Kerze). Auf der Oberfläche der T-Zelle gibt es für beide Signale spezifische Rezeptoren (hier: Augen/Blickkontakt):
 Die T-Helferzellen reichen die Information über das Vorliegen eines Gefahr (Kerze) und über die genaue Art der Gefahrenquelle, also das Antigen (Augenbinde des Bakteriums), über Rezeptoren und Signalstoffe (Sprechblase) an B-Zellen weiter und regen diese so zur Produktion spezifischer Antikörper an:
Die T-Helferzellen reichen die Information über das Vorliegen eines Gefahr (Kerze) und über die genaue Art der Gefahrenquelle, also das Antigen (Augenbinde des Bakteriums), über Rezeptoren und Signalstoffe (Sprechblase) an B-Zellen weiter und regen diese so zur Produktion spezifischer Antikörper an:
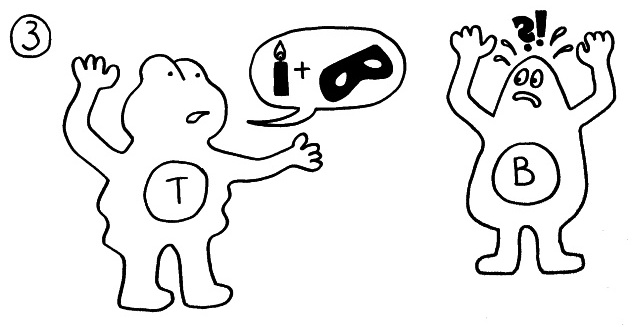 Die B-Zellen schütten massenhaft Antikörper aus (Eimer), die spezifisch an „ihr“ Antigen binden und die Gefahrenquellen so zum Teil direkt schachmatt setzen, zum Teil zur anschließenden Zerstörung und Entsorgung markieren:
Die B-Zellen schütten massenhaft Antikörper aus (Eimer), die spezifisch an „ihr“ Antigen binden und die Gefahrenquellen so zum Teil direkt schachmatt setzen, zum Teil zur anschließenden Zerstörung und Entsorgung markieren:
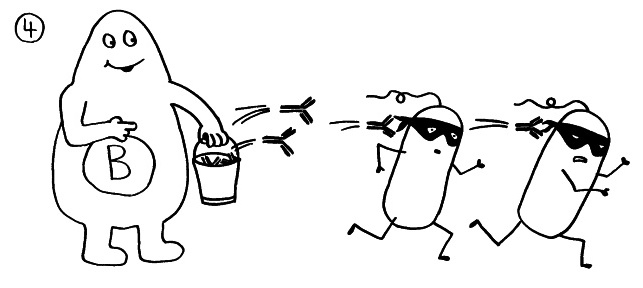 Diese normale Immunreaktion spielt sich in der Blutbahn, im Lymphgewebe und lokal im infizierten Gewebe ab. Aber manchmal läuft etwas schief: Aktivierte T-Zellen können die Blut-Nerven-Schranke durchdringen und von der Blutbahn (im nächsten Bild links) in einen Nerv (rechts) überwechseln. Das sollte eigentlich nicht passieren, da Nerven zu den sogenannten immunprivilegierten Orten im Körper gehören: Da Entzündungsreaktionen hier viel Schaden anrichten können, sind diese Orte für die meisten Immunzellen tabu. Weiterlesen
Diese normale Immunreaktion spielt sich in der Blutbahn, im Lymphgewebe und lokal im infizierten Gewebe ab. Aber manchmal läuft etwas schief: Aktivierte T-Zellen können die Blut-Nerven-Schranke durchdringen und von der Blutbahn (im nächsten Bild links) in einen Nerv (rechts) überwechseln. Das sollte eigentlich nicht passieren, da Nerven zu den sogenannten immunprivilegierten Orten im Körper gehören: Da Entzündungsreaktionen hier viel Schaden anrichten können, sind diese Orte für die meisten Immunzellen tabu. Weiterlesen
Hashimoto-Thyreoiditis und Morbus Basedow: neue Risikogenorte identifiziert
Jason D. Cooper et al.: Seven newly identified loci for autoimmune thyroid disease. Hum. Mol. Genet. 2012, doi: 10.1093/hmg/dds357 (Accepted manuscript, Open Access)
Zusammenfassung noch nicht allgemein verständlich aufbereitet
Abstract: Der ImmunoChip ist ein von zwölf Autoimmunforschergruppen und dem Wellcome Trust entwickelter Chip für die schnelle Durchmusterung von DNA-Proben auf 186 mit zwölf Autoimmunerkrankungen assoziierte SNPs (Einzelnukleotidpolymorphismen) und weitere von den Forschergruppen benannte „Kandidaten“ für Genorte, die mit den Erkrankungen assoziiert sein könnten. Hier wurden mit dem Chip 103.875 relativ häufige SNPs (Allelfrequenz mindestens 5 Prozent) aus 2285 Morbus-Basedow-Patienten, 462 Hashimoto-Patienten und 9364 Kontrollpersonen durchgetestet. Dabei wurden sieben neue Risiko-Genorte aufgespürt, von denen fünf auch mit anderen Autoimmunerkrankungen assoziiert sind. Weiterlesen
Würmer im Darm regen IL-10-Ausschüttung an und verhindern so bei Mäusen Typ-1-Diabetes
P. K. Mishra et al.: Prevention of type 1 diabetes through infection with an intestinal nematode parasite requires IL-10 in the absence of a Th2-type response. Mucosal Immunology, 18. Juli 2012, doi: 10.1038/mi.2012.7
Notizen noch nicht allgemeinverständlich zusammengefasst
Abstract: Wurminfektionen können Typ-1-Diabetes verhindert; Mechanismen noch unklar. Hier wurden NOD-Mäuse (Tiermodell für Typ-1-Diabetes), die kein Interleukin 4 produzieren können (IL-4-/-), im Alter von 5-7 Wochen mit dem Darmparasiten Heligmosomoides polygyrus infiziert und anschließend entwurmt. Im Unterschied zu den nicht infizierten Tieren entwickelten die meisten von ihnen bis zur 40. Lebenswoche keinerlei Anzeichen für Typ-1-Diabetes oder eine Schädigung der Betazellen in der Bauchspeicheldrüse. Die CD4+-STAT6-Phosphorylierung (also der IL-4/IL-13-Signalweg) war unterbunden, die CD4+-STAT1-Phosphorylierung (also die IFN-γ-Produktion) nicht. In FoxP3–-CD4+-T-Zellen war die IL-10-Produktion stark erhöht.
Blockierte man die IL-10-Signalgebung in den NOD-IL-4-/--Mäusen, so wurden die Betazellen zerstört, und die Tiere bekamen Typ-1-Diabetes. NOD-Mäuse, die IL-4 herstellen konnten, blieben dagegen auch bei einer IL-10-Signalblockade gesund. Ein Transfer jener CD4+-T-Zellen aus infizierten NOD-IL-4-/--Mäusen, die offenbar primär für die erhöhte IL-10-Produktion verantwortlich sind, in nicht infizierte NOD-IL-4-/--Mäuse verhinderte deren Erkrankung. Diese Zellen sind keine klassischen regulatorischen T-Zellen oder Tregs (kaum FoxP3). Weiterlesen
Mikrobiom und Autoimmunerkrankungen, V
Lora V. Hooper et al.: Interactions Between the Microbiota and the Immune System. Science 336(6086), 1268-1273, DOI: 10.1126/science.1223490
(Notizen nur zu den Teilen, in denen es um AIE geht)
In Tiermodellen, in denen Tregs fehlen, fördern Th1- und Th17-Zellen sowie IL-23-abhängige lymphoide Zellen der angeborenen Immunabwehr (innate lymphoid cells = ILCs) Colitis. Vermutlich werden auch beim Menschen CEDs durch ein Ungleichgewicht zwischen den verschiedenen Immunzelltypen ausgelöst, das wiederum von den Kommensalen beeinflusst wird. Dafür sprechen z. B. die starke Kopplung von Morbus Crohn an IL23R-Polymorphismen und von schwerer Enterocolitis an IL10– und IL10R-Mutationen.
Bei keimfrei aufgezogenen Mäusen ist der Verlauf von Arthritis, EAE (MS-Modell) oder Colitis i. A. schwerer als bei Mäusen mit normalem Mikrobiom. Bei Tiermodellen für Th17-abhängige Arthritis und EAE reicht eine Assoziation mit segmentierten filamentösen Bakterien (SFB) aus, um die Krankheit auszulösen. In all diesen Modellen hat die Vermehrung der Th17-Zellen im Darmschleimhaut-Immunsystem systemische Auswirkungen. Die Antigenspezifität dieser Zellen muss noch geklärt werden. Weiterlesen