Achtung, lang – aber am Ende ist man wirklich schlauer!
Ein schwieriges Thema
Viele Menschen mit Autoimmunerkrankungen leiden unter Schmerzen, die ihre Lebensqualität erheblich mindern und schwer zu bekämpfen sind. Ich bin von starken Schmerzen in den letzten Jahren zum Glück weitgehend verschont geblieben und hatte – wohl auch deshalb – in meinem Buch kein Kapitel über die Zusammenhänge zwischen Schmerz und Autoimmunstörungen vorgesehen. Schließlich ist mein Thema ohnehin schon furchtbar vielschichtig, auch wenn man die Wechselwirkungen zwischen dem (gesunden oder entgleisten) Immunsystem und dem (intakten oder beschädigten) Nervensystem ausklammert.
Aber dann erreichte mich eine ziemlich verzweifelte Anfrage von jemandem, der gerade höllische Schmerzen durchlitt und einen Zusammenhang mit einer Autoimmunerkrankung vermutete. Zwar konnte ich ihm leider nicht helfen; ich gebe grundsätzlich keine Diagnose- oder Therapieempfehlungen ab, da das meine Kompetenzen weit überschreiten würde. Aber mein Interesse war geweckt, und ungefähr zur selben Zeit wies mich ein Freund auf eine gute neue Übersichtsarbeit zu Schmerz bei Autoimmunerkrankungen hin. Und so habe ich mich doch in dieses Feld gestürzt, viel dazu gelesen, mit der fremden Fachterminologie gekämpft und einiges gelernt.
Was ist Schmerz?
Intuitiv weiß jeder, was mit Schmerz gemeint ist, aber es hilft ungemein, sich die genaue Definition anzusehen. Die Internationale Gesellschaft zur Erforschung des Schmerzes (IASP) spricht von einem „unangenehmen, heftigen Sinnes- und Gefühlserlebnis, das mit tatsächlichen oder potenziellen Gewebeschäden einhergeht“. Schmerz ist also kein unmittelbarer Sinnesreiz, sondern das Ergebnis einer aufwändigen Signalverarbeitung in der Peripherie (also etwa am Ort der auslösenden Verletzung), im Rückenmark und im Gehirn. An dieser Signalverarbeitung beteiligen sich neben den Nervenzellen oder Neuronen auch die sogenannten Gliazellen (ein Sammelbegriff für alle Zellen im zentralen Nervensystem, die keine Neuronen sind) und, wie sich inzwischen gezeigt hat, etliche Zellen des Immunsystems.
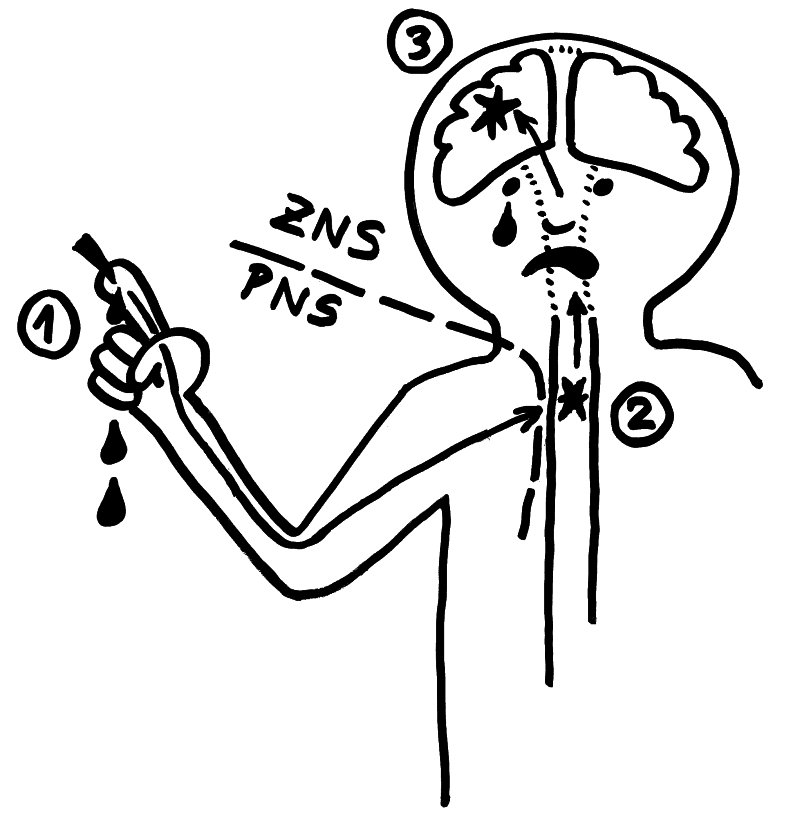
An der Schmerzentstehung sind die Nervenendigungen im peripheren Nervensystem (1), das Hinterhorn des Rückenmarks (2) und das Gehirn (3) beteiligt. Das Rückenmark zählt zum zentralen Nervensystem.
Etwas enger gefasst ist ein dem Schmerz verwandter Begriff, die Nozizeption. Noxen (vom lateinischen nocere = schaden) sind potenziell schädliche Reizauslöser physikalischer, chemischer, mikrobieller oder auch psychosozialer Natur, also etwa Hitze, ätzende Stoffe oder Krankheitserreger. Deren rein sinnesphysiologische, also ohne Beteiligung von Bewusstsein oder Gefühlen erfolgende Wahrnehmung (Perzeption) im zentralen Nervensystem (ZNS) heißt Nozizeption.
Die Alarmsignale, die im ZNS ankommen, gehen von spezialisierten freien Nervenendigungen in der Peripherie aus, also zum Beispiel in der Haut eines Fingers, in den sich gerade ein Dorn gebohrt hat. Diese für Schmerzreize empfindlichen Nervenendigungen, die Nozizeptoren, registrieren die Gewebeschädigung und senden dann elektrische Signale aus.