Fortsetzung meiner Notizen zum Buch, Kapitel 3: angeborene Abwehr
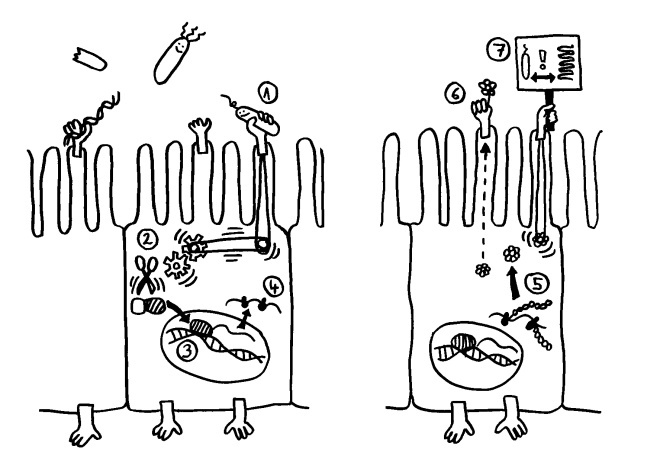
Modularität: Abwehrsysteme bestehen aus 3 Teilen: 1. Information über gefährliche Lage (lösliche extrazell. Rezeptormoleküle und zellassoziierte Sensoren), 2. Befehls- und Steuerungskomplex (Signalketten), 3. Effektoren (Enzyme, ROS etc.), die gut dosiert und verwahrt werden müssen, da sie auch eigenes Gewebe zerstören. Ausnahme: „smart weapons“ wie konstitutiv exprimierte kationische antimikrobielle Peptide, die an anionische Mikroben-Oberfläche binden und dann mit hydrophober Domäne in die Membran eindringen.
Evolution der Rezeptoren: in angeb. Abwehr alle möglichen Proteine, während sie in der erw. Abwehr alle zur Immunglobulin-Superfamilie gehören. Vielfalt über Jahrmillionen selektiert, für Pathogene schwerer auszuschalten als eine einzelne Proteinfamilie. Keimbahn-codiertes „phylogenetisches Pathogen-Gedächtnis“. Gene für erfolgreiche Rezeptorstrukturen oftmals dupliziert -> neue Bindungseigenschaften -> Familien. Viele Rezeptoren bestehen aus 2 oder mehr funktionalen Modulen.