Anhedonie: Lustlosigkeit, z. B. verringerte Libido
Wenn wir krank sind, uns ins Bett legen, fiebern und nichts essen mögen: ist das schlecht für uns? Ist es nur ein Zeichen dafür, dass es uns schlecht geht? Oder ist es vielmehr gut für uns, ein Teil unserer Genesung? Erstaunlich lange blieb diese Frage unbeantwortet. Erst 1988 veröffentlichte Benjamin L. Hart seine wegweisende Arbeit „Biological basis of the behavior of sick animals“, in der er das Krankheitsverhalten (sickness behavior) von Tieren als evolutionäre Anpassung zur effizienten Überwindung von Infektionskrankheiten darstellte.
Zu diesem Krankheitsverhalten zählen etwa
- Anorexie (verringerter Appetit)

Anorexie: verringerter Appetit

Adipsie: verringerter Durst
- Lethargie und Schläfrigkeit

Schläfrigkeit, Schonhaltung, Wärmeverlust-Minimierung
- Anhedonie (Lustlosigkeit, Unfähigkeit zur Freude, siehe oben: keinen Bock aufs Haserl!)
- Rückzug und Asozialität (verringerte Revierverteidigung, Brutfürsorge, wechselseitige Körperpflege, sexuelle Aktivität usw.)

reduziertes Sozialverhalten
- Desinteresse am Erkunden der Umgebung, am Spielen und Lernen
- Übelkeit, Unwohlsein
- erhöhte Schmerzempfindlichkeit
- bei Warmblütern Zittern zur Wärmeproduktion und bei wechselwarmen Tieren das Aufsuchen einer warmer Umgebung („behavioral fever“) sowie

„Verhaltensfieber“ bei wechselwarmen Tieren
- eine kompakte Körperhaltung, die den Wärmeverlust minimiert.
Hinzu kommen physiologische Veränderungen, etwa eine vom Hypothalamus im Gehirn angeordnete Erhöhung der Körpertemperatur (Fieber), Entzündungsreaktionen und eine träge Verdauung.
Noch immer glauben viele Menschen, Fieber sollte gesenkt werden und Brandwunden müsse man kühlen, weil die Wärme schädlich sei. Dabei dient beides „nur“ der Schmerzbekämpfung, nicht aber der Heilung – von Ausnahmen abgesehen. Zwar ist bei weitem nicht bei jeder Erkrankung klar, auf welchen Wegen Fieber uns nützt (Beschleunigung enzymatischer Reaktionen, Hemmung der Vermehrung hitzeempfindlicher Viren oder Bakterien, Entfernung des für Pathogene wichtigen Spurenelements Eisen aus unserem Blut …). Aber dass es eine Anpassungsleistung darstellt und in vielen Situationen das Überleben fördert, ist mittlerweile klar. So hatten in Tierexperimenten gezielt infizierte Wüstenleguane oder Zebrafische, die eine wärmere Umgebung aufsuchen konnten, eine deutlich höhere Überlebenswahrscheinlichkeit als Leidensgenossen, die man daran hinderte.
Viele der oben genannten Aspekte des Krankheitsverhaltens hängen miteinander zusammen. So rufen die Entzündungsreaktionen, mit denen unser Immunsystem Infektionen bekämpft, im Wachzustand Übelkeit, Abgeschlagenheit, Schmerz usw. hervor, die unsere Aktivitäten stören und riskanter machen können. Daher der Rückzug und der viele Schlaf. Der Rückzug von sozialen Aktivitäten könnte auch die Gefahr verringern, verwandte Artgenossen anzustecken. Andererseits kennen wir von vielen Tierarten Fürsorge für erkrankte Gruppenmitglieder, was darauf hindeutet, dass das verringerte Sozialverhalten und die Lethargie nicht dem Schutz der anderen, sondern der eigenen Genesung dienen, etwa der Konzentration der Energiereserven auf die kostspieligen Aktivitäten des Immunsystems.
Ob die verfügbare Energie eher in die Heilung oder doch in die kurzfristige Maximierung des Fortpflanzungserfolgs investiert wird, hängt wesentlich von der „life history“ und der Reproduktionsstrategie der Art ab: Kurzlebige kranke Säugetiermännchen paaren sich im Zweifel lieber noch einmal und kippen dann tot um. Langlebige Organismen schonen sich lieber; zur Not vernachlässigen sie ihre Jungen und setzen darauf, dass sie nach ihrer Genesung neuen Nachwuchs großziehen können.
Bei einer akuten Erkrankung fördert ein solches Krankheitsverhalten die Gesundung und damit die Chance, das Erbgut, in das dieses Verhalten eingeschrieben ist, in die nächsten Generationen weiterzutragen. So funktioniert natürliche Auslese. Bei chronischen Erkrankungen ist dasselbe Verhalten oftmals kontraproduktiv, denn ich kann nicht jahrelang hungern, die Tage verdämmern, enthaltsam leben und die sozialen Bedürfnisse meiner Mitgeschöpfe ignorieren, ohne mir selbst und meinen Verwandten zu schaden. Außerdem werden viele chronische Erkrankungen, etwa Autoimmunerkrankungen, wohl gar nicht durch Bakterien oder Viren verursacht, die sich durch ein solches Verhalten besiegen ließen.
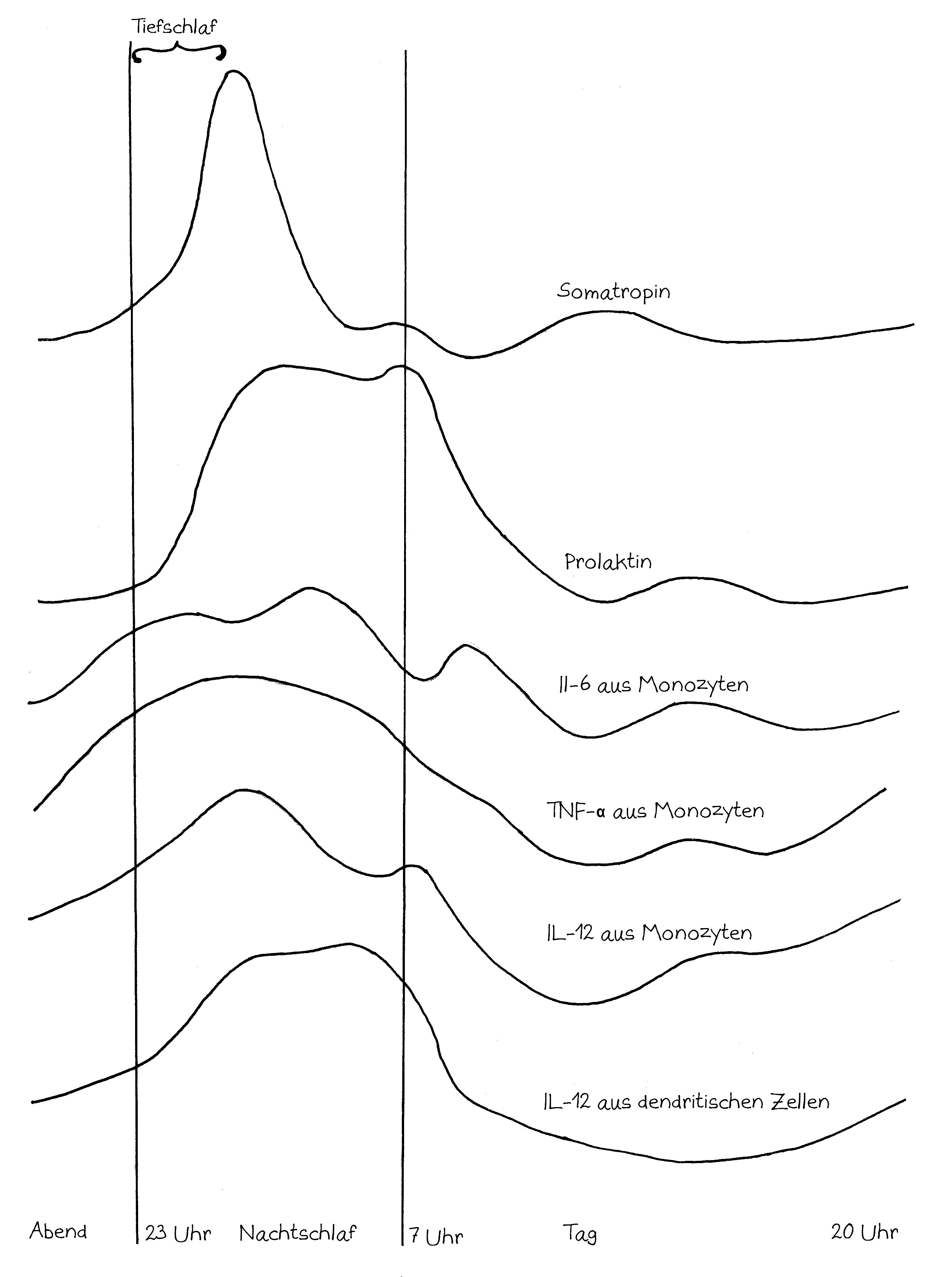
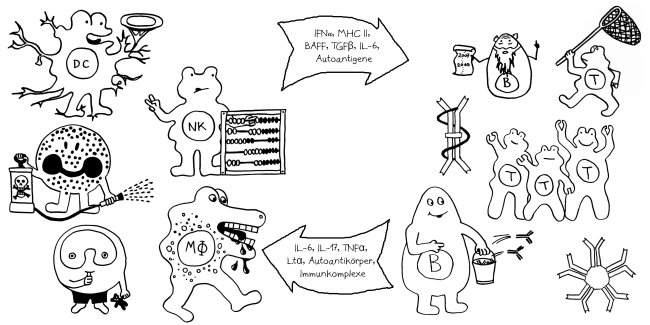
Da aber etliche chronische Erkrankungen erst gegen Ende oder gar nach der Reproduktionsphase auftreten, hat die natürliche Auslese keinen Ansatzpunkt, um einem solchen „chronifizierten Krankheitsverhalten“ entgegenzuwirken. Das einmal entgleiste Immunsystem, das fälschlich meint, eine Infektion bekämpfen zu müssen, schüttet permanent entzündungsfördernde Botenstoffe wie Interleukin 1β (IL-1β), Interleukin 6 (IL-6) und Tumornekrosefaktor (TNF) aus, die dem Hypothalamus und anderen Schaltzentralen suggerieren, der Organismus müsse noch ein Weilchen kürzer treten und sich zurückziehen. Das könnte der Grund für ein Phänomen sein, das vielen chronisch Kranken nur allzu bekannt ist: Fatigue.